Вариант 23
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют на внешнем энергетическом уровне два электрона. Запишите в поле ответа номера выбранных элементов.
1. N
2. Fe
3. As
4. Mg
5. P
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одной группе. Расположите выбранные элементы в порядке возрастания энергии ионизации. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
1. N
2. Fe
3. As
4. Mg
5. P
Из числа указанных в ряду элементов выберите два элемента, которые не проявляют отрицательную степень окисления. Запишите в поле ответа номера выбранных элементов.
1. N
2. Fe
3. As
4. Mg
5. P
Из предложенного перечня выберите два соединения, в которых присутствует ионная химическая связь.
1. CaBr2
2. NO
3. ВаО
4. HBr
5. NO2
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Al(OH)2NO3
Б) Аl(Н2РO4)
В) KAl(SO4)2
КЛАСС/ГРУППА
1) кислая соль
2) основная соль
3) смешанная соль
4) двойная соль
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует хлор.
1. серная кислота
2. раствор NaOH
3. фторид калия
4. хлорид железа(II)
5. хлорид меди(II)
Из предложенного перечня выберите два оксида, которые не реагируют с соляной кислотой.
1. Na2O
2. SiO2
3. BeO
4. CO
5. BaO
Краткое ионное уравнение реакции
2Н+ + S2- = H2S
описывает взаимодействие соли X с веществом Y.
Из предложенного перечня выберите два вещества, которые могут вступать в описанную реакцию.
1. HNO2
2. HCl
3. CuS
4. Al2S3
5. K2S
Задана следующая схема превращений веществ: Na →X→ Na2O2 →Y→ Na2СО3 Определите, какие из указанных веществ являются веществами X и Y.
1. H2O2
2. NaOH
3. O2
4. K2CO3
5. CO2
Установите соответствие между уравнением реакции и изменением степени окисления восстановителя в ней: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УРАВНЕНИЕ РЕАКЦИИ
А) 2Аl + 3S = Al2S3
Б) SO2 + Br2 = SO2Br2
В) S + O2 = SO2
Г) 3S + 6KOH = 2K2S + K2SO3 + 3H2O
ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ВОССТАНОВИТЕЛЯ
1) 0 → +2
2) 0 → +3
3) 0 → +4
4) -2 → +4
5) +4 → +6
6) +2 → +6
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Н2
Б) Na2O
В) Сг(ОН)3
Г) СаСО3
РЕАГЕНТЫ
1) НСl, SiO2, Аl2O3
2) С, Сг2O3, ВаСl2
3) HNO3, NaOH, СН3СООН
4) СО, ZnO, НВг
5) O2, Na, С2Н2
Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) этин
Б) ацетон
В) 2-аминобутан
КЛАСС/ГРУППА
1) кетоны
2) амины
3) аминокислоты
4) углеводороды
Из предложенного перечня веществ выберите два вещества, которые являются межклассовыми изомерами.
1) бутанол-1
2) цис-бутен-2
3) транс-бутеи-2
4) бутановая кислота
5) метилпропиловый эфир
Из предложенного перечня выберите два углеводорода, при гидратации которых образуется кетон.
1) этин
2) этен
3) пентен-1
4) бутин-2
5) бутин-1
Из предложенного перечня выберите два вещества, с которыми взаимодействует глицерин.
1) этен
2) гидроксид меди(II)
3) гидроксид железа(III)
4) бутан
5) азотная кислота
Из предложенного перечня выберите два вещества, каждое из которых может образовывать дипептиды.
1) анилин
2) глицерин
3) аминоуксусная кислота
4) пропил амин
5) аланин
Задана следующая схема превращений веществ:
пропин →X→ пропанол-2 →Y→ 2-бромпропан
Определите, какие из указанных веществ являются веществами Х и Y.
1) пропаналь
2) пропанон
3) бромид калия
4) бромоводородная кислота
5) бром
Установите соответствие между схемой реакции и её продуктом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) 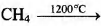
Б) СН3 — СН3 + HNO3 →
В) 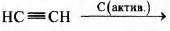
Г) 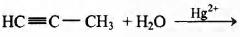
ПРОДУКТ
1) бензол
2) пропанон
3) ацетилен
4) этиламин
5) пропанол
6) нитроэтан
Установите соответствие между протекающей реакцией и продуктом, который образуется в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАКЦИЯ
А) окисление ацетальдегида
Б) гидрирование ацетальдегида
В) дегидратация метанола
Г) гидролиз метилата калия
ПРОДУКТ
1) CН3СНО
2) CН3СООН
3) HCHO
4) CH3CH2OH
5) CH3OCH3
6) CH3OH
Из предложенного перечня выберите две экзотермические реакции.
1) взаимодействие алюминия с соляной кислотой
2) разложение хлорида аммония
3) разложение гидроксида железа(III)
4) взаимодействие метана с хлором
5) взаимодействие азота с кислородом
Из предложенного перечня выберите две реакции, для которых увеличение давления приведет к увеличению скорости взаимодействия.
1) СаСO3 + 2НВr(p-p) → СаВr2 + СО2 + Н2О
2) СН2 = СН2 + Н2 → СН3 — СН3
3) Fe + I2(тв.) → Fel2
4) Fe + 2НВr(г) → FeBr2 + Н2
5) КН + Н2О → КОН + Н2
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) Ag2SO4
Б) K3PO4
В) CuCl2
Г) K2S
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и сера
2) водород и кислород
3) металл и галоген
4) металл и кислород
5) водород и сера
Установите соответствие между названием соли и средой водного раствора этой соли: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ СОЛИ
А) нитрат аммония
Б) сульфат натрия
В) фосфат натрия
Г) сульфид бария
СРЕДА РАСТВОРА
1) нейтральная
2) кислая
3) щелочная
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при понижении давления в системе: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца.
УРАВНЕНИЕ РЕАКЦИИ
A) C3H8(r) [math]\leftrightarrows[/math] C3H6(r) + H2(r) - Q
Б) C3H7OH(r) [math]\leftrightarrows[/math] C3H6(r) + H2O(r) - Q
В) FeCl2(p-p) + H2O(ж) [math]\leftrightarrows[/math] Fe(OH)Cl(p-p) + HCl(p-p) - Q
Г) 2CO2(r) [math]\leftrightarrows[/math] 2CO(r) + O2(r) - Q
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) в сторону продуктов реакции
2) в сторону исходных веществ
3) практически не смещается
Установите соответствие между формулами реагирующих веществ и признаком их взаимодействия: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) HI и AgNO3
Б) Ca(NO3)2 и Na2CO3
В) FeCl3 и NaOH
Г) СаСО3 И HNO3 (конц.)
ПРИЗНАК РЕАКЦИИ
1) образование желтого осадка
2) образование белого осадка
3) образование бурого осадка
4) выделение бесцветного газа
5) выделение бурого газа
Установите соответствие между веществом и областью его применения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) O3
Б) HC [math]\equiv[/math] CH
В) NaCl
Г) C4H10
ОБЛАСТЬ ПРИМЕНЕНИЯ
1) обеззараживание воды
2) в качестве бытового газа
3) получение хлорвинила
4) производство удобрений
5) консервант в пищевой промышленности
Какую массу воды (в граммах) надо добавить к 150 г раствора с массовой долей глюкозы 20% для получения раствора с массовой долей 15%?
Ответ:___________________г.
(Запишите число с точностью до целых.)
В результате реакции, термохимическое уравнение которой
3Fe + 2O2 = Fe3O4 + 1200 кДж,
выделилось 240 кДж теплоты. Найдите объем кислорода (в литрах, н.у.), вступившего в реакцию.
Ответ:___________________л.
(Запишите число с точностью до целых.)
Вычислите массу альдегида (в граммах), который образуется при окислении 9,2 г этанола оксидом меди(II).
Ответ:___________________г.
(Запишите число с точностью до десятых.)
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции
... + NH3 → МnО2 + N2 + ... + Н2О
Определите окислитель и восстановитель.
Электронный баланс:
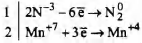
Окислитель Мn+7 (или КМnO4), восстановитель N-3 (или NH3).
Уравнение реакции
2КМnO4 + 2NH3 → 2МnO2 + N2 + 2КОН + 2Н2O
Кристаллический иод обработали концентрированной азотной кислотой при нагревании, наблюдая выделение бурого газа. Образовавшуюся кислоту осторожно нагрели, при этом получился ангидрид этой кислоты. Полученный ангидрид прореагировал с угарным газом, а выделившееся простое вещество прореагировало с металлическим железом. Напишите уравнения четырёх описанных реакций.
1) I2 + 10HNO3(конц.) = 2НIO3 + 10NO2 + 4Н2O
2) 2НIO3 = I2O5 + Н2O
3) I2O5 + 5СО = I2 + 5СО2
4) Fe + I2 = Fel2
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
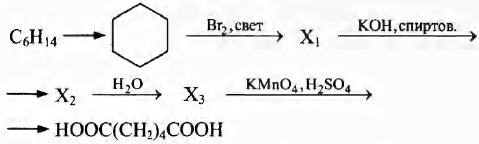
При написании уравнений реакций используйте структурные формулы органических веществ.
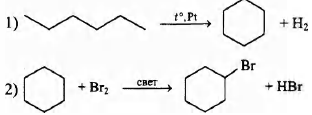
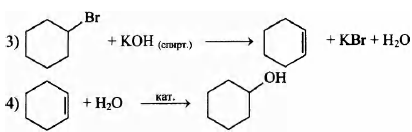
5) 5C6Н11ОН + 8KMnO4 + 12H2SO4 → 5НООС—(СН2)4—СООН + 8MnSO4 + 4K2SO4 + 17Н2O
Избыток оксида меди(II) нагрели с 3,36 л (н.у.) водорода. В результате реакции получили 10,4 г твёрдого остатка. Этот остаток полностью растворился в 150 г 75%-ной серной кислоты. Определите массовую долю соли в полученном растворе.
w(CuSO4) = 0,170 или 17,0%.
Органическое вещество X может быть получено взаимодействием некоторого углеводорода Y с избытком брома (при использовании недостатка брома возможно образование других веществ, являющихся по отношению друг к другу структурными изомерами). При сжигании образца вещества X получено 2,24 л (н.у.) углекислого газа, 0,45 г воды и 8,1 г бромоводорода.
На основании данных условия задания:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества X;
3) составьте возможную структурную формулу вещества X, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции получения вещества X взаимодействием углеводорода Y с избытком брома.
2) молекулярная формула вещества С4Н6Вr4
3) структурная формула СН2Вг—СНВr—СНВr—СН2Вr
4) уравнение реакции
СН2 = СН — СН = СН2 + 2Вг2 → СН2Вг — СНВг — СНВг — СН2Вг
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||