Вариант 29
Часть 1.
При выполнении заданий 1–15 укажите только одну цифру, которая соответствует номеру правильного ответа.
Фосфид-иону соответствует схема заполнения электронных слоёв
1) 2; 8; 5
2) 2; 8; 8
3) 8; 8; 2
4) 5; 8; 6
В каком ряду химические элементы расположены в порядке уменьшения числа валентных электронов?
1) Li, Be, В
2) S, Р, С
3) К, Na, Li
4) С, Si, Ge
В каком ряду записаны вещества только с ионной связью?
1) сероуглерод, вода, нашатырь
2) хлорид натрия, сульфид железа (II), нитрид натрия
3) фосфат калия, сероводород, аммиак
4) угарный газ, аргон, медь
Значения высшей и низшей степеней окисления углерода соответственно равны
1) +2 и -4
2) +2 и +4
3) +4 и -2
4) +4 и -4
Двухосновной кислотой является
1) хлорная
2) ортофосфорная
3) кремниевая
4) метафосфорная
Признаком химической реакции карбоната кальция с соляной кислотой является
1) образование осадка
2) свечение
3) выделение газа
4) появление запаха
Уравнением электролитической диссоциации является
1) СаСO3 [math]\rightleftarrows[/math]СаO + CO2
2) NH4Cl [math]\rightleftarrows[/math] NH3 + НСl
3) CH3COONa + Н2O [math]\rightleftarrows[/math] СН3СООН + NaOH
4) Н3РO4 [math]\rightleftarrows[/math] Н+ + Н2[math]РО_4^-[/math]
С каким веществом реагирует нитрат меди(II) согласно сокращённому уравнению реакции Cu2+ + S2- = CuS?
1) сероводородом
2) сульфидом натрия
3) сульфитом натрия
4) сульфидом свинца
Не происходит выделение свободного галогена при взаимодействии
1) I2 и КВr
2) Вr2 и Nal
3) Сl2 и КВr
4) Сl2 и Nal
С кислотными оксидами реагируют все вещества в группе
1) Al2O3, Cl2O, ZnO
2) MgO, SO3, СО
3) SO2, P2O3, СO2
4) К2O, FeO, Сr2O3
С гидроксидом кальция реагирует каждое из двух веществ:
1) оксид меди(II) и гидроксид алюминия
2) оксид углерода(IV) и фосфорная кислота
3) йодоводород и кислород
4) хлороводородная кислота и водород
Хлорид аммония вступает в реакцию с
1) гидроксидом кальция
2) раствором азотной кислоты
3) азотом
4) раствором бромида бария
Верны ли следующие суждения о чистых веществах и смесях?
А. Сливочное масло является чистым веществом.
Б. Чугун является смесью веществ.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
В уравнении окислительно-восстановительной реакции
Fe3O4 + Аl → Аl2O3 + Fe
коэффициент перед формулой окислителя равен
1) 2
2) 4
3) 3
4) 8
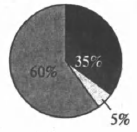
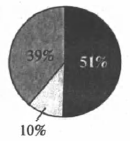
На какой диаграмме распределение массовых долей элементов отвечает качественному составу нитрата аммония?
1) 
2) 
3) 
4) 
При выполнении заданий 16, 17 из предложенного перечня ответов выберите два правильных и запишите в таблицу цифры, под которыми они указаны.
В ряду химических элементов As → Р → N:
1) увеличивается электроотрицательность
2) возрастают радиусы атомов
3) усиливаются металлические свойства
4) уменьшается валентность в высших оксидах
5) увеличивается термическая устойчивость водородных соединений
В состав животных жиров преимущественно входят остатки
1) глицерина
2) высших непредельных карбоновых кислот
3) высших предельных карбоновых кислот
4) метанола
5) этиленгликоля
При выполнении заданий 18, 19 к каждому элементу первого первого столбца подберите соответствующий элемент из второго столбца. Запишите выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
ВЕЩЕСТВА
А) СаСO3 и Са3(РO4)2
Б) NH4NO3 и AgNO3
В) Pb(NO3)2 и AgNO3
РЕАКТИВ
1) H2O
2) HCl
3) FeS
4) Cu
Установите соответствие между названием вещества и реагентами, с каждым из которых оно может взаимодействовать.
НАЗВАНИЕ ВЕЩЕСТВА
А) азот
Б) кальций
В) бром
ФОРМУЛЫ РЕАГЕНТОВ
1) O2, SO2
2) МnСl2, N2
3) H2, Li
4) NaOH, CuSO4
Часть 2.
Для ответов на задания 20—22 используйте отдельный лист. Запишите сначала номер задания (20, 21, 22), а затем развернутый ответ к нему. Ответы записывайте четко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции
Na2CrO4 + Nal + H2SO4 → I2 + Cr2(SO4)3 + Na2SO4 + H2O.
Определите окислитель и восстановитель.
Na2Cr+6O4 + Nal+ + H2SO4 → [math]I_2^0[/math] + [math]Cr_2^+3[/math](SO4)3 + Na2SO4 + H2O
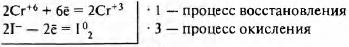
2Сr+6 + 6I- = 2Сr+3 + [math]3I_2^0[/math]
Cr+6(Cr+32(SO4)3) — окислитель
I-(NaI-) — восстановитель
Молекулярное уравнение
2Na2CrO4 + 6NaI + 8H2SO4 = 3I2 + Cr2(SO4)3 + 5Na2SO4 + 8H2O
При обжиге известняка массой 300 г был получен оксид углерода(IV) массой 100 г. Определите массовую долю (в процентах) карбоната кальция в известняке.
1) Уравнение реакции:
CaCO3 = CaO + CO2↑.
2) Рассчитываем количество вещества CO2:
М(СO2) = 44 г/моль, n(CO2) = 100/44 ≈ 2,27 моль.
3) Рассчитываем массовую долю СаСO3 в известняке:
а) по уравнению реакции
n(СаСO3) = n(СO2) = 2,27 моль СаСO3
М(СаСO3) = 100 г/моль, m(СаСO3) = 2,27 • 100 = 227 г
б) m(СаСO3) = 227 • 100/300 ≈ 75,67 %.
Даны вещества: ZnO, Zn, растворы MgSO4, H2SO4, AgNO3, Ba(NO3)2. Используя воду и необходимые вещества только из этого списка, получите в две стадии нитрат цинка. Опишите признаки проводимых реакций. Для реакции ионного обмена напишите сокращённое ионное уравнение реакции.
Схема эксперимента Zn → H2SO4 → Zn(NO3)2
1) Zn + H2SO4 = ZnSO4 + H2↑
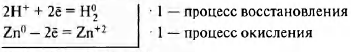
Zn0+ 2Н+ = Zn2+ + [math]Н_2^0[/math]
H+(H2SO4) — окислитель
Zn0 — восстановитель
Реакция окислительно-восстановительная. Цинк растворяется и выделяется газообразный водород.
2) ZnSO4 + Ba(NO3)2 = Zn(NO3)2 + BaSO4↓
Ba2+ + [math]SO_4^2-[/math] = BaSO4
Образуется белый осадок сульфата бария. Реакция ионного обмена
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||