Вариант 8
Часть 1.
При выполнении заданий 1–15 укажите только одну цифру, которая соответствует номеру правильного ответа.
На приведенном рисунке
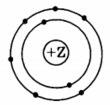
изображена модель атома
1) углерода
2) кислорода
3) серы
4) кремния
В подгруппах Периодической системы с увеличением заряда ядра атомов происходит
1) усиление неметаллических свойств элементов
2) уменьшение числа протонов в ядре
3) увеличение радиуса атомов
4) увеличение электроотрицательности
Ковалентная неполярная связь реализуется в
1) молекуле оксида углерода(IV)
2) молекуле S8
3) кристаллическом льде
4) молекуле NH3
Степень окисления +4, а валентность IV атом углерода проявляет в соединении
1) СН4
2) CO
3) H2CO3
4) Al4C3
В перечне веществ:
А) Na2SiO3
Б) H2SiO3
В) KCIO3
Г) NH4Cl
Д) NH3 • H2O
Е) H2S
к солям относятся:
1) АБВ
2) ВГД
3) ГДЕ
4) АВГ
Если в бесцветный раствор хлорида ртути(II) поместить кусочек меди красного цвета, то произойдет реакция:
1) обмена
2) соединения
3) разложения
4) замещения
К сильным электролитам относится каждое из двух веществ
1) NaOH и С2Н5ОН
2) Са(ОН)2 и Н2СO3
3) AgNO3 и Ва(ОН)2
4) AlCl3 и H2S
Практически полностью в водном растворе взаимодействуют вещества:
1) КОН и Fe2(SO4)3
2) NaOH и Ba(NO3)2
3) Na2SO4 и КСl
4) К3РO4 и NaCl
И кислород, и водород реагируют с
1) аммиаком
2) хлором
3) серной кислотой
4) натрием
Оксид углерода(IV) реагирует с каждым из двух веществ:
1) Н2O и СаО
2) O2 и Na2O
3) КОН и Na2SO4
4) Fe2O3 и H2SO4
Среди веществ, формулы которых Fe, Сu, Mg, в реакцию с холодной концентрированной серной кислотой вступает(-ют)
1) Mg и Сu
2) только Сu
3) Fe и Mg
4) Fe, Сu и Mg
В отличие от сульфата натрия сульфат меди реагирует с
1) гидроксидом магния
2) хлоридом бария
3) нитратом кальция
4) гидроксидом калия
Верны ли следующие суждения о правилах безопасной работы в химической лаборатории?
А. Метан образует взрывчатые смеси с воздухом.
Б. Растворять серную кислоту следует, добавляя к ней воду.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
В уравнении окислительно-восстановительной реакции
NH3 + O2 → Н2O + NO
коэффициент перед формулой окислителя равен
1) 6
2) 5
3) 4
4) 3
На какой диаграмме распределение массовых долей элементов соответствует составу нитрата калия?

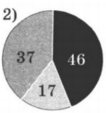


При выполнении заданий 16, 17 из предложенного перечня ответов выберите два правильных и запишите в таблицу цифры, под которыми они указаны.
В ряду химических элементов О — S — Se
1) уменьшается радиус атомов
2) увеличивается значение высшей степени окисления
3) увеличивается сила кислот Н2Э
4) уменьшается электроотрицательность
5) увеличивается число внешних электронов
Метанол реагирует с
1) калием
2) карбонатом натрия
3) бромом
4) гидроксидом меди(II)
5) кислородом
При выполнении заданий 18, 19 к каждому элементу первого первого столбца подберите соответствующий элемент из второго столбца. Запишите выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества. К каждому элементу первого столбца подберите соответствующий элемент второго столбца.
ВЕЩЕСТВА
А) Fe и Ag
Б) СаО и СаСО3
В) NH3(p-p) и NH4Cl(p-p)
РЕАКТИВ
1) фенолфталеин
2) Na2SO4(p-p)
3) HCl(p-p)
4) KNO3(p-p)
Установите соответствие между исходными веществами и продуктами реакции.
ИСХОДНЫЕ ВЕЩЕСТВА
А) НСl + Fe
Б) H2SO4 + Fe2O3
В) HNO3(конц.) + Cu
ПРОДУКТЫ РЕАКЦИИ
1) FeCl2 + H2
2) FeCl3 + Н2
3) Fe2(SO4)3 + H2O
4) Cu(NO3)2 + H2
5) Cu(NO3)2 + NO2 + H2O
Часть 2.
Для ответов на задания 20—22 используйте отдельный лист. Запишите сначала номер задания (20, 21, 22), а затем развернутый ответ к нему. Ответы записывайте четко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции
CuSO4 + KI → K2SO4 + Cul + I2
Определите окислитель и восстановитель.
1. Составлен электронный баланс.
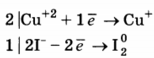
2. Расставлены коэффициенты в уравнении реакции:
2CuSO4 + 4KI = 2K2SO4 + 2CuI +I2
3. Указано, что восстановителем является I-, а окислителем Сu+2.
При растворении в разбавленной серной кислоты образца цинка, содержащего 4,5% нерастворимых примесей, выделилось 2,24 л (н.у.) водорода. Определите массу образца металла.
1) Уравнение реакции:
Zn + H2SO4 = ZnSO4 + H2↑
2) Рассчитываем количество вещества H2:
n(H2) = V/Vm =2,24л/22,4л/моль = 0,1 моль
3) Рассчитываем массу Zn(чист.):
а) по уравнению реакции: n(Zn(чист.)) = n(H2) = 0,1 моль
б) M(Zn) = 65 г/моль, m(Zn(чист.)) = n*M = 0,1 моль * 65 г/моль = 6,5 г
4) Рассчитываем массовую долю (Zn(чист.)):
ω(Zn(чист.)) = 100% - 4,5% = 95,5%
5) Рассчитываем массу образца металла:
m(Zn) = m(Zn(чист.))/ω(Zn(чист.)) = 6,5г/0,955 ≈ 6,8 г
Для проведения эксперимента предложены следующие реактивы: алюминий, карбонат натрия и растворы соляной кислоты, хлорида алюминия и гидроксида натрия. Вам также предоставлен комплект лабораторного оборудования, необходимый для проведения химических реакций.
Требуется получить гидроксид алюминия в результате проведения двух последовательных реакций. Выберите необходимые для этого реактивы из числа тех, которые вам предложены. Составьте схему превращений, в результате которых можно получить указанное вещество. Запишите уравнения двух реакций. Для первой реакции составьте сокращённое ионное уравнение.
Составлена схема превращений, в результате которой можно получить гидроксид алюминия:
1) Аl → АlСl3 → Аl(ОН)3
Составлены уравнения двух проведённых реакций
2) 2Аl + 6НСl = 2АlСl3 + ЗН2 ↑
3) АlСl3 + 3NaOH = Аl(ОН)3 ↓ + 3NaCl
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||