Вариант 3
Часть 1.
При выполнении заданий 1–15 укажите только одну цифру, которая соответствует номеру правильного ответа.
На приведенном рисунке
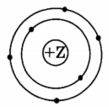
изображена модель атома
1) кремния
2) серы
3) кислорода
4) углерода
Порядковый номер химического элемента в Периодической системе Д.И. Менделеева соответствует:
1) числу электронов в атоме
2) значению высшей валентности элемента по кислороду
3) числу электронов, недостающих до завершения внешнего электронного слоя
4) числу электронных слоев в атоме
Ионной связью образовано каждое из двух веществ:
1) хлорид бария и нитрид лития
2) фосфин и аммиак
3) оксид углерода(II) и оксид бария
4) оксид углерода(IV) и оксид фосфора(V)
Азот проявляет одинаковую степень окисления в каждом из двух веществ, формулы которых:
1) N2O5 и LiNO3
2) Li3N и NO2
3) NO2 и HNO2
4) NH3 и N2O3
К кислотным оксидам относится каждое из двух веществ:
1) СO2, СаО
2) SO2, CO
3) SO2, P2O5
4) P2O5, Al2O3
Выпадение осадка голубого цвета является признаком реакции между веществами:
1) гидроксидом натрия и соляной кислотой
2) карбонатом калия и хлоридом кальция
3) сульфатом аммония и хлоридом бария
4) нитратом меди (II) и гидроксидом бария
Хлорид-ионы образуются при электролитической диссоциации
1) КСlO4
2) KClO3
3) CH3Cl
4) KCl
Взаимодействию соляной кислоты и едкого натра отвечает краткое ионное уравнение
1) НСl + ОН- = Н2O + Cl
2) Н+ + ОН- =Н2O
3) Н+ + NaOH = Н2O + Na+
4) Н+ + Сl+ОН =Н2O + Сl-
Алюминий образует сульфат алюминия при взаимодействии с
1) серой
2) серной кислотой
3) сернистой кислотой
4) сероводородом
Оксид железа(II) взаимодействует с раствором
1) аммиака
2) бромоводорода
3) карбоната калия
4) хлорида натрия
И с серебром, и с оксидом меди(II) будет реагировать
1) соляная кислота
2) фосфорная кислота
3) азотная кислота
4) угольная кислота
Хлорид железа(II) в водном растворе может реагировать с
1) K2S
2) CO2
3) SiO2
4) Cu
Верны ли следующие суждения об обращении с растворами щелочей?
А. При попадании раствора щелочи на кожу рук его надо смыть водой, а затем обработать раствором борной кислоты.
Б. При попадании раствора щелочи на кожу рук его надо смыть раствором соды.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
В уравнении окислительно-восстановительной реакции
MnO + Аl → Аl2O3 + Мn
коэффициент перед формулой восстановителя равен
1) 1
2) 2
3) 3
4) 4
Массовая доля азота в нитрате алюминия равна
1) 14,0%
2) 19,7%
3) 6,6%
4) 21,3%
При выполнении заданий 16, 17 из предложенного перечня ответов выберите два правильных и запишите в таблицу цифры, под которыми они указаны.
Общим для фосфора и серы является
1) наличие трех электронных слоев в их атомах
2) значение их электроотрицательности меньше, чем у хлора
3) образование ими водородных соединений с общей формулой ЭН2
4) образование ими простых веществ в виде двухатомных молекул
5) одинаковые значения степени окисления в кислородных соединениях.
С уксусной кислотой взаимодействуют вещества, формулы которых
1) H2SiO3
2) Na2CO3
3) Hg
4) Cu(OH)2
5) BaSO4
При выполнении заданий 18, 19 к каждому элементу первого первого столбца подберите соответствующий элемент из второго столбца. Запишите выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между веществами и реактивом, с помощью которого можно различить эти вещества. К каждому элементу первого столбца подберите соответствующий элемент из второго столбца.
ВЕЩЕСТВА
А) АlСl3(р-р) и ВаСl2(р-р)
Б) СuСl2(р-р) и CuSO4(p-p)
В) Аl(ОН)3(тв.) и Са3(РO4)2(тв.)
РЕАКТИВ
1) AgNO3(p-p)
2) фенолфталеин
3) КСl
4) NaOH(p-p)
Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать.
НАЗВАНИЕ ВЕЩЕСТВА
А) оксид углерода(IV)
Б) гидроксид калия
В) сульфат меди(II)
РЕАГЕНТЫ
1) Fe2(SO4)3(p-p), H2SiO3
2) Mg, NaOH(p-p)
3) CaSO4, H2O
4) BaCl2(p-p), Fe
Часть 2.
Для ответов на задания 20—22 используйте отдельный лист. Запишите сначала номер задания (20, 21, 22), а затем развернутый ответ к нему. Ответы записывайте четко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции
PbS + HNO3 → PbSO4 + NO + Н2O
Определите окислитель и восстановитель.
1. Составлен электронный баланс.
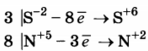
2. Расставлены коэффициенты в уравнении реакции:
3PbS + 8HNO3 = 3PbSO4 + 8NO + 4Н2O
3. Указано, что восстановителем является S-2 , а окислителем N+5.
Рассчитайте массу осадка, который образуется при взаимодействии раствора карбоната калия с раствором нитрата бария массой 17,4 г с массовой долей соли 15%.
1) Уравнение реакции:
K2CO3 + Ba(NO3)2 = 2KNO3 + BaCO3↓
2) Рассчитываем массу Ba(NO3)2 в растворе:
m(Ba(NO3)2) = ω(Ba(NO3)2)*m(р-ра)= 0,15 * 17,4 г = 2,61 г
3)Рассчитываем количество вещества Ba(NO3)2:
M(Ba(NO3)2) = 261 г/моль, n(Ba(NO3)2) = m/M = 2,61г/261г/моль = 0,01 моль
4)Рассчитываем массу BaCO3:
а) по уравнению реакции: n(BaCO3) = n(Ba(NO3)2) = 0,01 моль
б) M(BaCO3) = 197 г/моль, m (BaCO3) = n*M = 0,01 моль * 197 г/моль = 1,97 г
Даны вещества: Zn, НСl(разб.), Fe, К3РO4, NaOH, СаСO3. Используя воду и необходимые вещества только из этого списка, получите в две стадии ортофосфат кальция. Опишите признаки проводимых реакций. Для первой реакции напишите сокращённое ионное уравнение.
Составлены два уравнения реакции:
1) СаСO3 + 2НСl = СаСl2 + Н2O + СO2 ↑
2) ЗСаСl2 + 2К3РO4 = Са3(РO4)2 ↓ + 6КСl
Описаны признаки протекания реакций:
3) для первой реакции: выделение бесцветного газа;
4) для второй реакции: образование белого осадка.
Составлено сокращённое ионное уравнение первой реакции:
5) СаСO3 + 2Н+ = Са2+ + Н2O + СO2 ↑
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||