Вариант 14
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
Определите, атомы каких из указанных в ряду элементов содержат во внешнем слое два электрона.
1) Ba
2) Na
3) Be
4) S
5) Si
1) Ba 2) Na 3) Fe 4) S 5) Si
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде. Расположение выбранные элементы в порядке возрастания основности их высших оксидов. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
1) Ba 2) Na 3) Fe 4) S 5) Si
Из числа указанных в ряду элементов выберите два элемента, которые проявляют степень окисления +4. Запишите в поле ответа номера выбранных элементов.
Из предложенного перечня выберите два соединения, в которых химическая связь образована за счет общей пары электронов.
1. Ca
2. H2O
3. NaCl
4. CaO
5. Cl2
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) ВеО
Б) Na2O2
В) ВаО
КЛАСС/ГРУППА
1) пероксид
2) оксид основный
3) оксид амфотерный
4) оксид несолеобразующий
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует натрий.
1. водород
2. сульфат калия
3. оксид алюминия
4. пероксид натрия
5. метан
Из предложенного перечня выберите два оксида, которые реагируют с кислородом.
1. оксид меди(II)
2. оксид железа(II)
3. оксид фосфора(V)
4. оксид углерода(II)
5. оксид углерода(IV)
В пробирку с раствором вещества X добавили несколько капель соли Y. В результате реакции произошло выделение газа с неприятным запахом. Из предложенного перечня выберите два вещества, которые могут вступать в описанную реакцию.
1. КОН
2. НСl
3. CuSO4
4. Na2CO3
5. K2S
Задана следующая схема превращений веществ:
[math]H_2SO_3\xrightarrow{X_1}H_2SO_4\xrightarrow{X_2}NaHSO_4[/math]
Определите, какие из указанных веществ являются веществами Х1 и X2.
1. SO2
2. NaOH
3. Br2(p-p)
4. NaNO3(p-p)
5. Na2S
Установите соответствие между схемой реакции и изменением степени окисления восстановителя в ней. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) С2Н2 + Н2 → С2Н4
Б) НСООН + Сl2 → СO2 + НСl
В) NH4Cl + NaNO2 → N2 + NaCl + H2O
Г) NaNO3 → NaNO2 + O2
ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ВОССТАНОВИТЕЛЯ
1) от -3 до 0
2) от -2 до 0
3) от -1 до 0
4) от 0 до +1
5) от +2 до +4
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Сl2
Б) Аl2O3
В) Са(ОН)2
Г) NaHSO3
РЕАГЕНТЫ
1) NaOH, NaCl, HF
2) H2SO4, NaOH, HBr
3) NaHSO4, Br2, SO2
4) NaBr, Ba(OH)2, Fe
5) C6H6, KI, NaOH
Установите соответствие между названием вещества и классом группой, к которому(ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) CH3COCH3
Б) CH3OCH3
В) CH3COOCH3
КЛАСС/ГРУППА
1) простой эфир
2) сложный эфир
3) альдегид
4) кетон
Из предложенного перечня выберите два вещества, в молекулах которых все атомы углерода находятся в состоянии sp2-гибридизации
1. ацетилен
2. этилен
3. этанол
4. стирол
5. циклопентан
Из предложенного перечня выберите два вещества, с которыми реагирует толуол.
1. HNO3
2. Н2O
3. Сl2
4. НСl
5. H2SO4
Из предложенного перечня выберите два вещества, с которыми реагирует глицерин, но не реагирует фенол.
1. K
2. H2
3. HCl
4. NaOH
5. Cu(OH)2
Из предложенного перечня выберите два вещества, с которыми реагирует этиламин.
1. соляная кислота
2. оксид магния
3. хлорид натрия
4. гидроксид натрия
5. хлорметан
Задана следующая схема превращений веществ:
этилен [math]\xrightarrow X[/math] этанол [math]\xrightarrow Y[/math] бромэтан
Определите, какие из указанных веществ являются веществами X и Y.
1. КОН
2. НВr
3. Вr2
4. Н2O
5. NaBr
Установите соответствие между углеводородом и продуктом, который преимущественно образуется при его взаимодействии с бромом в соотношении 1:1. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УГЛЕВОДОРОД
А) пропен
Б) пропин
В) циклопропан
Г) 2-метилпропан
ПРОДУКТ РЕАКЦИИ
1) 2-метил-2-бромпропан
2) 1,2-дибромпропан
3) 2-бромпропан
4) 1,3-дибромпропан
5) 1,2-дибромпропен
6) 2,2-дибромпропан
Установите соответствие между веществом и углеродсодержащими продуктом реакции, который преимущественно образуется при взаимодействии этого вещества с оксидом меди(II): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) уксусная кислота
Б) этанол
В) метанол
Г) пропанол-2
ПРОДУКТ РЕАКЦИИ
1) ацетон
2) ацетальдегид
3) формальдегид
4) пропаналь
5) формиат меди(II)
6) ацетат меди(II)
Из предложенного перечня выберите два типа реакций, к которым можно отнести взаимодействие муравьиной кислоты с этиловым спиртом.
1. нейтрализации
2. обратимая
3. присоединения
4. каталитическая
5. гетерогенная
Из предложенного перечня выберите две реакции, для которых увеличение давления приведет к увеличению скорости реакции.
1. СаСО3 + 2НСl → СаСl2 + СO2 + Н2O
2. СН2=СН2 + Н2 → СН3-СН3
3. Н2 + Сl2 → 2HCI
4. Mg + 2НСl → MgCl2 + Н2
5. КН + Н2O → КОН + Н2
Установите соответствие между формулой соли и продуктами электролиза её водного раствора, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) Al(NO3)3
Б) LiCl
В) Cu(NO3)2
Г) NaF
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород и кислород
2) металл и кислород
3) водород и галоген
4) металл и галоген
5) металл и водород
Установите соответствие между названием соли и отношением этой соли к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ СОЛИ
А) сульфат аммония
Б) нитрат натрия
В) ацетат магния
Г) фосфат натрия
ОТНОШЕНИЕ К ГИДРОЛИЗУ
1) гидролиз по катиону
2) гидролиз по аниону
3) гидролиз по катиону и аниону
4) гидролизу не подвергается
Установите соответствие между фактором, действующим на равновесную систему
СН3СООН(ж) + СН3ОН(ж) [math]\rightleftarrows[/math] СН3СООСН3(ж) + H2O(ж)и направлением смещения химического равновесия в этой системе: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФАКТОР
А) добавление метанола
Б) повышение давления
В) повышение концентрации эфира
Г) добавление гидроксида натрия
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) смещается в сторону прямой реакции
2) смещается в сторону обратной реакции
3) смещение равновесия не происходит
Установите соответствие между формулами веществ и реагентом, с помощью которого можно различить их водные растворы: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛЫ ВЕЩЕСТВ
А) NH3 и Н2
Б) Аl и Mg
В) Аl(ОН)3 и Mg(OH)2
Г) NaCl и NaHSO3
РЕАГЕНТ
1) NaOH
2) H2SO4
3) фенолфталеин
4) NaBr
5) BaO
Установите соответствие между смесью и способом ее разделения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СМЕСЬ
А) жидкость и нерастворимая твердая примесь
Б) две взаиморастворимые жидкости
В) несмешивающиеся жидкости
Г) жидкость и растворимая твердая примесь
СПОСОБ РАЗДЕЛЕНИЯ
1) с помощью делительной воронки
2) выпариванием
3) фильтрованием
4) перегонкой
Смешали 160 г раствора с массовой долей нитрата кальция 15% и 40 г раствора с массовой долей этой же соли 20%. Чему равна масса соли в полученном растворе? (Запишите число с точностью до целых.)
Ответ: ______________г
При полном окислении 1 г глюкозы C6H12O6 выделяется 17,6 кДж теплоты. Какое количество теплоты выделяется при окислении 1 моль глюкозы? (Запишите число с точностью до целых.)
Ответ: ____________ кДж
Рассчитайте объём (н.у.) газа, выделяющегося при действии серной кислоты на 10 г сульфида алюминия. (Запишите число с точностью до сотых.)
Ответ: ___________________л.
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции:
Cr2(SO4)3 + Сl2 + ... → K2CrO4 + KCl + ... + H2O
Определите окислитель и восстановитель.
Элементы ответа:
1) Составлен электронный баланс:
[math]2\;\vert\;Cr^{+3}\;-\;3\overline e\rightarrow Cr^{+6}[/math]
[math]3\;\vert\;Cl_2^0+2\overline e\rightarrow2Cl^-[/math]
2) Указано, что сульфат хрома(III) (за счёт хрома в степени окисления +3) является восстановителем, а хлор в степени окисления 0 - окислителем.
3) Определены недостающие в схеме вещества, и расставлены коэффициенты в уравнении реакции:
Cr2(SO4)3 + 3CI2 + 16КОН = 2К2СrO4 + 6KCI + 3K3SO4 + 8Н2O
Карбид алюминия полностью растворили в бромоводородной кислоте. К полученному раствору добавили раствор сульфита калия, при этом наблюдали образование белого осадка и выделение бесцветного газа. Газ поглотили раствором дихромата калия в присутствии серной кислоты. Образовавшуюся соль хрома выделили и добавили к раствору нитрата бария, наблюдали выделение осадка. Напишите уравнения четырёх описанных реакций.
1) AI4C3 + 12НВr = 4АlВr3 + ЗСН4↑
2) 2АlВr3 + 3K2SO3 + ЗН2O = 2Аl(ОН)3↓ + 3SO2↑ + 6КВr
3) 3SO2 + К2Сr2O7 + H2SO4 = Cr2(SO4)3 + K2SO4 + Н2O
4) Cr2(SO4)3 + ЗВа(NO3)2 = 3BaSO4↓ + 2Сr(NO3)3
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
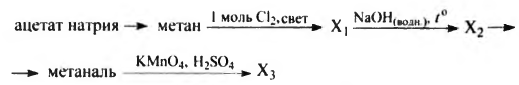
При написании уравнений реакций используйте структурные формулы органических веществ.
1) CH3COONa + NaOH [math]\xrightarrow{t^\circ}[/math] CH4 + Na2CO3
2) CH4 + CI2 [math]\xrightarrow{light}[/math] CH3Cl + HCl
3) CH3Cl + NaOH(водн.) [math]\xrightarrow{t^\circ}[/math] CH3OH + NaCl
4) CH3OH + CuO [math]\xrightarrow{t^\circ}[/math] CH2O + Cu + H2O
5) 5CH2O + 4KMnO4 + 6H2SO4 [math]\xrightarrow{}[/math] 5CO2 + 4MnSO4 + 2K2SO4 + 11H2O
Газ, выделившийся при взаимодействии 7,4 г нитрида кальция с 9 г воды, полностью поглощён 200 мл 3,5%-ного раствора соляной кислоты (р = 1,05 г/мл). Определите массовую долю хлорида аммония в образовавшемся растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения физических величин).
1) Составлены уравнения реакций:
Са3N2 + 6Н2O = ЗСа(ОН)2 + 2NH3
NH3 + НСl = NH4CI
2) Определено количество вещества NH3, и указано, что вода дана в избытке: n(Ca3N2) = 7,4/148 = 0,05 моль
n(Н2O) = 9 /18 = 0,5 моль, следовательно, Н2O - в избытке.
n(NH3) = 2n(Ca3N2) = 0,1 моль
3) Определено количество вещества NH4Cl, и указано, что НСl в избытке:
n(НСl) = 200 • 1,05 • 0,035 / 36,5 = 0,2 моль
НСl - в избытке
n(NH3) = n(NH4Cl) = 0,1 моль
4) Определена массовая доля NH4Cl:
m(NH4Cl) = 0,1 • 53,5 = 5,35 г
w(NH4Cl) = 5,35 / 200 • 1,05 + 17 • 0,1 = 0,025, или 2,5%
При сгорании 4,48 л (н.у.) газообразного органического вещества получили 35,2 г углекислого газа и 10,8 мл воды. Плотность этого вещества составляет 2,41 г/л (н.у.). Известно также, что это вещество не реагирует с аммиачным раствором оксида серебра, а при реакции его с избытком бромной воды происходит присоединение атомов брома только ко вторичным атомам углерода.
На основании данных условия задачи:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества;
3) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции этого вещества с избытком бромной воды.
Общая формула вещества - CxHyOz
1) Найдены количество вещества углекислого газа, воды и органического вещества:
n(СO2) = 35,2 / 44 = 0,8 моль
n(Н2O) = 10,8 /18 = 0,6 моль
M(CxHyOz) = 2,41 * 22,4 = 54 г/моль
n(CxHyOz) = 4,48 / 22,4 = 0,2 моль
2) Определена молекулярная формула вещества:
n(С) = n(СO2) = 0,8 моль
n(Н) = 2n(Н2O) = 1,2 моль
х = n(С) / n(CxHyOz) = 0,8 / 0,2 = 4
у = n(H) / n(CxHyOz) = 1,2 / 0,2 = 6
4 • 12 + 6 + z • 16 = 30
z = 0
Молекулярная формула - С4Н6
3) Составлена структурная формула вещества:
[math]СН_3С\equiv ССН_3[/math]
4) Составлено уравнение реакции этого вещества с избытком бромной воды:

| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||