Вариант 4
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
1) Na 2) N 3) Si 4) Р 5) С
Определите, атомы каких из указанных в ряду элементов имеют в основном состоянии два неспаренных электрона. Запишите в поле ответа номера выбранных элементов.
Расположите в порядке увеличения числа неспаренных электронов на внешнем уровне в основном состоянии химические элементы:
1. C
2. P
3. Al
Степени окисления азота в нитрате аммония равны:
1. -3
2. -2
3. +3
4. +4
5. +5
Атомную кристаллическую решётку в твёрдом состоянии имеют:
1. кислород
2. белый фосфор
3. красный фосфор
4. алмаз
5. хлорид натрия
Установите соответствие между формулой вещества и классом, к которому это вещество принадлежит: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца.
ФОРМУЛА ВЕЩЕСТВА
А) NH4Fe(SO4)2
Б) Са(СlO)Сl
В) NO2
КЛАСС
1) соль двойная
2) оксид кислотный
3) оксид амфотерный
4) соль смешанная
Из предложенного перечня веществ выберите два вещества, с каждым из которых может реагировать углерод.
1. углекислый газ
2. сульфат натрия (р-р)
3. разбавленная азотная кислота
4. концентрированная соляная кислота
5. оксид железа(III)
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует углекислый газ.
1. оксид железа(III)
2. оксид кальция
3. концентрированная азотная кислота
4. гидроксид хрома(III)
5. гидроксид калия
Фосфат аммония реагирует в водном растворе с:
1. H2SO4
2. NaOH
3. KNO3
4. NH3
5. SiO2
В заданной схеме превращений
[math]Ca(H_2PO_4)_2\xrightarrow XCa_3(PO_4)_2\xrightarrow YP_4[/math]
веществами X и Y соответственно являются:
1. Ca(OH)2
2. Н2O
3. Ca
4. C
5. H2SO4
Установите соответствие между схемой реакции и формулой окислителя в ней.
СХЕМА РЕАКЦИИ
А) NaOH + Br2 → NaBr + NaOBr + Н2O
Б) Вr2 + O2 → ВrO2 + O2
В) Сl2 + I2 → ICl
Г) НСl + НСlO3 → Сl2 + Н2O
ФОРМУЛА ОКИСЛИТЕЛЯ
1) NaOH
2) Br2
3) Cl2
4) I2
5) HClO3
6) O3
Установите соответствие между исходными веществами и продуктами их взаимодействия.
ИСХОДНЫЕ ВЕЩЕСТВА
А) Na2CO3 + Н3РO4 →
Б) Na2CO3 + Н2СO3 →
В) Na3PO4 + Н2СO3 →
Г) Na + Н3РO4 →
ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ
1) Na3PO4 + Н2O + СO2
2) Na2HPO4 + Na2CO3
3) Na3PO4 + Н2
4) NaH2PO4 + Н2
5) NaHCO3
6) Na2HPO4 + H2O + CO2
Установите соответствие между формулой органического соединения и его названием.
ФОРМУЛА СОЕДИНЕНИЯ
А) СН3—ОН
Б) С6Н5—СН=СН2
В) СН2(OН)—СН2(OН)
Г) CH2=CH—CH=CH2
НАЗВАНИЕ СОЕДИНЕНИЯ
1) дивинил
2) метанол
3) изопрен
4) этандиол
5) толуол
6) стирол
Гомологами являются:
1. изобутан и 2-метилпентан
2. стирол и пропанол-2
3. этилбензол и о-ксилол
4. этанол и пропанол-1
5. муравьиная и акриловая кислоты
Пентен-2, в отличие от пентана, реагирует с
1. водородом
2. хлором
3. аммиачным раствором оксида серебра
4. раствором перманганата калия
5. кислородом
Из предложенного перечня веществ выберите два вещества, с которыми реагирует фенол.
1. водород
2. азотная кислота
3. углекислый газ
4. 2,2-диметилпентан
5. сульфат алюминия
Из предложенного перечня выберите два вещества, с которыми реагирует аминоуксусная кислота, но не реагирует метиламин.
1. уксусная кислота
2. водород
3. кислород
4. аммиак
5. кальций
В заданной схеме превращений
фенолят натрия [math]\xrightarrow X[/math] фенол [math]\xrightarrow Y[/math] пикриновая кислота
веществами X и Y соответственно являются:
1. H2
2. HCl
3. KOH
4. HNO3
5. KNO3
Установите соответствие между реагирующими веществами и органическим продуктом, который преимущественно образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) толуол и хлор (FeCl3)
Б) толуол и хлор (свет)
В) бензол и водород
Г) бензол и хлорметан
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) хлористый бензил
2) циклогексан
3) толуол
4) метилгексахлорциклогексан
5) ксилол
6) хлортолуол
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) CH3COOK и КОН
Б) СН3СООН и СН3ОН
В) СН3ОН и К
Г) СН3ОН и H2SO4
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) диэтиловый эфир
2) метилацетат
3) метилат калия
4) метан
5) диметиловый эфир
6) метаналь
Взаимодействие железа с серой относится к реакциям:
1. некаталитическим
2. гетерогенным
3. эндотермическим
4. окислительно-восстановительным
5. обмена
Увеличение давления в системе в наибольшей степени скажется на скорости химической реакции между
1. азотом и водородом
2. железом и серной кислотой
3. сульфатом алюминия и раствором щёлочи
4. сернистым газом и кислородом
5. растворами серной кислоты и щёлочи
Установите соответствие между формулой вещества и продуктом, выделяющимся на аноде при электролизе водного раствора этого вещества.
ФОРМУЛА ВЕЩЕСТВА
А) NaF
Б) Hg(NO3)2
В) FeCl2
Г) KHSO4
АНОДНЫЙ ПРОДУКТ
1) кислород
2) металл
3) водород
4) сера
5) фтор
6) хлор
Установите соответствие между названием соли и средой ее водного раствора.
НАЗВАНИЕ СОЛИ
А) хлорид золота(III)
Б) сульфат железа(II)
В) ортофосфат цезия
Г) ацетат калия
СРЕДА РАСТВОРА
1) нейтральная
2) кислая
3) щелочная
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при уменьшении давления в системе:
УРАВНЕНИЕ РЕАКЦИИ
А) SO2Cl2(г) [math]\rightleftarrows[/math] SO2(г) + Cl2(г)
Б) 2SO2(г) + O2(г) [math]\rightleftarrows[/math] 2SO3(г)
В) 2HI(г) [math]\rightleftarrows[/math] H2(г) + I2(тв.)
Г) S(г) + H2(г) [math]\rightleftarrows[/math] H2S(г)
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) в сторону продуктов реакции
2) в сторону исходных веществ
3) практически не смещается
Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ВЕЩЕСТВА
А) СН3СООН + NaOH
Б) Zn(OH)2 + КОН (р-р)
В) КМnO4 + H2S
Г) АlСl3 + AgNO3
ПРИЗНАКИ РЕАКЦИИ
1) растворение осадка
2) образование осадка
3) изменение окраски раствора
4) выделение газа
5) видимых признаков реакции нет
На открытом пламени горелки нельзя нагревать колбу с:
1. 15%-ным раствором серной кислоты
2. водным раствором уксусной кислоты
3. спиртовым раствором КОН
4. раствором брома в гексане
5. раствором иода в тетрахлорметане
При упаривании 300 г 5%-ного раствора сахарозы получено 245 г раствора. Какова массовая доля сахарозы в нём? (Запишите число с точностью до целых.)
Ответ: ____________________%.
Рассчитайте максимально возможный объём (н.у.) аммиака, который может быть получен исходя из 40 л водорода и 30 л азота. (Запишите число с точностью до десятых.)
Ответ: ____________________л.
Сульфид железа(Н) массой 33,4 г обработали избытком хлороводородной кислоты. Определите объём (н.у.) газа, выделившегося в результате этой реакции. (Запишите число с точностью до десятых.)
Ответ: _____________л
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение
Cr2(SO4)3 + Cl2 + ... → K2CrO4 + KCl + ... H2O
Определите окислитель и восстановитель.
Элементы ответа:
1) Составлен электронный баланс:
[math]2\vert\;Cr^{+3}-3\overline e\rightarrow Cr^{+6}[/math]
[math]3\vert Cl\;_2^0+2\overline e\rightarrow2Cl^-[/math]
2) Указано, что сульфат хрома(III) (за счет хрома в степени окисления +3) является восстановителем, а хлор в степени окисления 0 - окислителем.
3) Определены недостающие в схеме вещества, и расставлены коэффициенты в уравнении реакции:
Cr2(SO4)3 + 3Cl2 + 16KOH = 2K2CrO4 + 6KCl + 3K2SO4 + 8H2O
Карбид алюминия полностью растворили в бромоводородной кислоте.
К полученному раствору добавили раствор сульфита калия, при этом наблюдали образование белого осадка и выделение бесцветного газа. Газ поглотили раствором дихромата калия в присутствии серной кислоты. Образовавшуюся соль хрома выделили и добавили к раствору нитрата бария, наблюдали выделение осадка.
Напишите уравнения четырёх описанных реакций.
1) [math]Al_4C_3+12HBr=4AlBr_3+3CH_4\uparrow[/math]
2) [math]2AlBr_3+3K_2SO_3+3H_2O=2Al(OH)_3\downarrow+3SO_2\uparrow+6KBr[/math]
3) [math]3SO_2+K_2Cr_2O_7+H_2SO_4=Cr2(SO_4)_3+K_2SO_4+H_2O[/math]
4) [math]Cr_2(SO_4)_3+3Ba(NO_3)_2=3BaSO_4\downarrow+2Cr(NO_3)_3[/math]
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
ацетат натрия [math]\rightarrow[/math] метан [math]\xrightarrow{1\;моль\;Cl_2,свет}X_1\xrightarrow{NaOH_{(водн)},t^\circ}X_2\rightarrow[/math] метаналь[math]\xrightarrow{KMnO_4,\;H_2SO_4}X_3[/math]При написании уравнений реакций используйте структурные формулы органических веществ.
Ответ включает в себя 5 уравнений реакций, соответствующих схеме превращений:
1) [math]CH_3COONa+NaOH\xrightarrow{t^\circ}CH_4+Na_2CO_3[/math]
2) [math]CH_4+Cl_2\rightarrow CH_3Cl+HCl[/math]
3) [math]CH_3Cl+NaOH\xrightarrow{t^\circ}CH_3OH+NaCl[/math]
4) [math]CH_3OH+CuO\xrightarrow{t^\circ}CH_2O+Cu+H_2O[/math]
5) [math]\begin{array}{l}5CH_2O+4KMnO_4+6H_2SO_4\rightarrow\\\rightarrow5CO_2+4MnSO_4+2K_2SO_4+11H_2O\end{array}[/math]
Газ, выделившийся при взаимодействии 7,4 г нитрида кальция с 9 г воды, полностью поглощён 200 мл 3,5%-ного раствора соляной кислоты (р = 1,05 г/мл). Определите массовую долю хлорида аммония в образовавшемся растворе.
Элементы ответа:
1) Составлены уравнения реакций:
Ca3N2 + 6H2O = 3Ca(OH)2 + 2HN3
NH3 + HCl = NH4Cl
2) Определено количество вещества NH3, и указано, что вода дана в избытке:
n(Ca3N2) = 7,4 / 148 = 0,05 моль
n(H2O) = 9 / 18 = 0,5 моль, следовательно, H2O - в избытке.
n(NH3) = 2n(Ca3N2) = 0,1 моль
3) Определено количество вещества NH4Cl, и указано, что HCl - в избытке:
n(HCl) = 200 x 1,05 x 0,035 / 36,5 = 0,2 моль
HCl - в избытке
n(NH3) - n(NH4Cl) = 0,1 моль
4) Определена массовая доля NH4Cl:
m(NH4Cl) = 0,1 x 53,5 = 5,35 г
ω(NH4Cl) = 5,35 / 200 x 1,05 + 17 x 0,1 = 0,025 или 2,5 %
При сгорании 4,48 л (н.у.) газообразного органического вещества получили 35,2 г углекислого газа и 10,8 мл воды. Плотность этого вещества составляет 2,41 г/л (н.у.). Известно также, что это вещество не реагирует с аммиачным раствором оксида серебра, а при реакции его с избытком бромной воды происходит присоединение атомов брома только ко вторичным атомам углерода.
На основании данных условия задачи:
1. произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2. запишите молекулярную формулу органического вещества;
3. составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4. напишите уравнение реакции этого вещества с избытком бромной воды.
Элементы ответа:
Общая формула вещества - CxHyOz
1) Найдены количество вещества углекислого газа, воды и органического вещества:
n(CO2) = 35,2 / 44 = 0,8 моль
m(H2O) = 10,8 / 18 = 0,6 моль
M(CxHyOz) = 2,41 x 22,4 = 54 г/моль
n(CxHyOz) = 4,48 / 22,4 = 0,2 моль
2) Определена молекулярная формула вещества:
n(C) = n(CO2) = 0,8 моль
n(H) = 2n(H2) = 1,2 моль
x = n(C) / n(CxHyOz) = 0,8 / 0,2 = 4
y = n(H) / n(CxHyOz) = 1,2 / 0,2 = 6
4 x 12 + 6 + z x 16 = 30
z = 0
Молекулярная формула C4H6
3) Составлена структурная формула вещества:
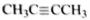
4) Составлено уравнение реакции этого вещества с избытком бромной воды:
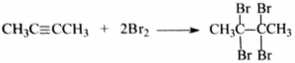
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||