Вариант 15
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
1) S 2) Zn 3) O 4) Ва 5) Se
Определите, атомы каких из указанных в ряду элементов не содержат неспаренных электронов. Запишите в поле ответа номера выбранных элементов.
1) S 2) Zn 3)O 4) Ва 5)Se
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одной группе. Расположите выбранные элементы в порядке возрастания кислотности образуемых ими летучих водородных соединений. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Степень окисления +2 могут проявлять оба элемента:
1. Mg и Сr
2. О и Аl
3. С и N
4. Mg и Р
5. S и Р
Из предложенного перечня выберите два соединения, между молекулами которых образуется водородная связь.
1. фенол
2. диэтиловый эфир
3. этилацетат
4. муравьиный альдегид
5. муравьиная кислота
Установите соответствие между формулой вещества и классом, к которому это вещество принадлежит: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца.
ФОРМУЛА ВЕЩЕСТВА
А) NH4F
Б) Са(ОН)2
В) Fe(OH)3
КЛАСС
1) соль
2) основание
3) амфотерный гидроксид
4) кислота
Из предложенного перечня выберите два вещества, с которыми реагирует белый фосфор.
1. NaOH
2. Аl(ОН)3
3. HCl
4. HNO3
5. СO2
Из предложенного перечня выберите два вещества, которые реагируют с углекислым газом.
1. Mg
2. SO3
3. NO
4. HCl
5. K2O
В пробирку с раствором соли X добавили несколько капель раствора вещества Y. В результате реакции наблюдали выделение желеобразного осадка. Из предложенного перечня выберите два вещества, которые могут вступать в описанную реакцию.
1. KOH
2. K2SiO3
3. H2SO4
4. LiBr
5. KNO3
Задана следующая схема превращений веществ:
[math]SiO_2\xrightarrow XK_2SiO_3\xrightarrow YBaSiO_3[/math]
Определите, какие из указанных веществ являются веществами X и Y.
1. H2O
2. BaCl2
3. KCl
4. BaSO4
5. K2O
Установите соответствие между формулой соли и степенью окисления хрома в ней.
ФОРМУЛА СОЕДИНЕНИЯ
А) К[СrO3Сl]
Б) Na2Cr2O7
В) CrOF
Г) Na3[Cr(OH)6]
СТЕПЕНЬ ОКИСЛЕНИЯ ХРОМА
1) 0
2) +2
3) +3
4) +4
5) +5
6) +6
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Li
Б) SO2
В) Zn(OH)2
Г) ZnBr2
РЕАГЕНТЫ
1) СаО,O2, КОН
2) Cl2, Na2CO3, LiOH
3) K2SO4, Р2O5, HNO3
4) Ва(ОН)2, КОН2, НСl
5) H2SO4, С2Н5ОН, N2
Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) нитроглицерин
Б) глицерин
В) аланин
КЛАСС/ГРУППА
1) спирт
2) аминокислота
3) сложный эфир
4) нитросоединение
Изомерами пентина-1 являются
1. пентен-1
2. циклопентан
3. пентадиен-1,3
4. изопрен
5. дивинил
Из предложенного перечня выберите два вещества, которые вступают в реакцию гидратации.
1. бензол
2. толуол
3. циклобутан
4. ацетилен
5. дивинил
Из предложенного перечня выберите два вещества, с которыми реагирует фенол.
1. Br2
2. HCl
3. KNO3
4. KOH
5. HCOOH
Из предложенного перечня выберите два вещества, которые являются менее сильным основанием, чем аммиак.
1. анилин
2. метиламин
3. диметиламин
4. дифениламин
5. метилэтиламин
Задана следующая схема превращений веществ:
[math]C_2H_6\xrightarrow XC_2H_5Br\xrightarrow YC_2H_4[/math]
Определите, какие из указанных веществ являются веществами X и Y.
1. КОН (спирт.)
2. H2O
3. Br2
4. NaOH (водн.)
5. HBr
Установите соответствие между схемой процесса и стадией цепной реакции, на которой происходит этот процесс. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА ПРОЦЕССА
А) СН4 + Сl• → СН3• + НСl
Б) •CH3 + •СН3 → СН3-СН3
В) Сl2 → 2Сl•
Г) •CCl3 + Cl• → ССl4
СТАДИЯ ЦЕПНОЙ РЕАКЦИИ
1) зарождение цепи
2) развитие цепи
3) обрыв цепи
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) уксусная кислота и гидросульфит натрия
Б) этиловый спирт и натрий
В) муравьиная кислота и оксид натрия
Г) этаналь и водород
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) ацетат натрия
2) этилат натрия
3) этанол
4) формиат натрия
5) уксусная кислота
6) углекислый газ
Из предложенного перечня выберите два вещества, термическое разложение которых является окислительно-восстановительной реакцией.
1. карбонат кальция
2. гидроксид меди(II)
3. нитрат железа(II)
4. оксид ртути(II)
5. кремниевая кислота
Из предложенного перечня выберите два внешних воздействия, которые приведут к увеличению скорости реакции
S(тв.) + O2(г) = SO2(г)
1. понижение температуры
2. добавление серы
3. измельчение серы
4. уменьшение концентрации кислорода
5. увеличение давления
Установите соответствие между формулой соли и продуктами электролиза её водного раствора, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) Al2(SO4)3
Б) MgCl2
В) Cu(NO3)2
Г) CuCl2
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород и кислород
2) металл и кислород
3) водород и галоген
4) металл и галоген
5) металл и водород
Установите соответствие между названием соли и средой ее водного раствора.
НАЗВАНИЕ СОЛИ
А) гидрокарбонат калия
Б) гидрофосфат натрия
В) ортофосфат цезия
Г) дигидрофосфат натрия
СРЕДА РАСТВОРА
1) нейтральная
2) кислая
3) щелочная
Установите соответствие между уравнением обратимой химической реакции и одновременным изменением внешних условий, приводящих к смещению химического равновесия в сторону продуктов реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УРАВНЕНИЕ РЕАКЦИИ
А) N2(г) + 3H2(г) [math]\rightleftarrows[/math] 2NH3(г) + Q
Б) N2O4(ж) [math]\rightleftarrows[/math] 2NO2(г) - Q
В) CO2(г) + C(тв.) [math]\rightleftarrows[/math] 2CO(г) + Q
Г) 4HCl(г) + O2 [math]\rightleftarrows[/math] 2H2O(г) + 2Cl2(г) + Q
ИЗМЕНЕНИЕ УСЛОВИЙ
1) увеличение температуры и давления
2) уменьшение температуры и давления
3) увеличение температуры и уменьшение давления
4) уменьшение температуры и увеличение давления
Установите соответствие между веществами и реагентом, с помощью которого их можно отличить друг от друга.
ВЕЩЕСТВА
А) BaSO4 и Са3(РO4)2
Б) ВаСl2 и MgCl2
В) AgNO3 и KNO3
Г) Na2O и MgO
РЕАГЕНТ
1) H2SO4(paзб.)
2) НСl(разб.)
3) H2O
4) NaNO3
5) HNO3(конц.)
Установите соответствие между аппаратом химической промышленности и процессом, протекающем в этом аппарате: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
АППАРАТ
А) ректификационная колонна
Б) колонна синтеза
В) контактный аппарат
Г) поглотительная башня
ПРОЦЕСС
1) синтез метанола
2) перегонка нефти
3) окисление сернистого газа
4) взаимодействие оксида серы(VI) с серной кислотой
5) очистка сернистого газа
К 280 г раствора с массовой долей бромида аммония 12% добавили 40 мл воды и 28 г этой же соли. Чему равна массовая доля соли в полученном растворе? (Запишите число с точностью до десятых.)
Ответ: _____________%
Согласно термохимическому уравнению реакции горения метана
СH4(г) + 2O2(г) = СO2(г) + 2Н2O(г) + 880 кДж
выделилось 2200 кДж теплоты. Определите количество вещества сгоревшего при этом метана. (Запишите число с точностью до десятых.)
Ответ: ______________моль
Чему равен объём водорода (н.у.), выделившийся при взаимодействии 3,75 моль цинка с избытком разбавленного раствора серной кислоты?(Запишите число с точностью до целых.)
Ответ: _________ л.
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции:
Na2SO3 + ... + H2SO4 → ... + MnSO4 + K2SO4 + Н2O
Определите окислитель и восстановитель.
1) Составлен электронный баланс:
[math]2\;\vert\;Mn^{+2}+5\overline e\rightarrow Mn^{+2}[/math]
[math]5\;\vert\;S^{+4}-2\overline e\rightarrow S^{+6}[/math]
2) Указано, что Na2SO3 (за счёт серы в степени окисления +4) является восстановителем, а КМnO4 (за счёт марганца в степени окисления +7) - окислителем.
3) Определены недостающие вещества, и расставлены коэффициенты в уравнении реакции:
5Na2SO3 + 2КМnO4 + 3H2SO4 = 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O
Натрий сожгли на воздухе. Образовавшееся вещество обработали концентрированной соляной кислотой. Полученное простое вещество при нагревании вступило в реакцию с оксидом хрома(III) в присутствии гидроксида калия. При обработке раствора одной из образовавшихся солей хлоридом бария выпал жёлтый осадок. Напишите уравнения четырёх описанных реакций.
1) 2Na + O2 = Na2O2
2) Na2O2 + 4HCl = 2NaCl + Cl2 + 2H2O
3) Cr2O3 + 3Cl2 + 10КОН [math]\xrightarrow{t^\circ}[/math] 2К2СrO4 + 6КСl + 5H2O
4) К2СrO4 + BaCl2 = ВаСrO4↓ + 2КСl
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
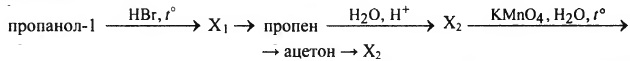
При написании уравнений реакций используйте структурные формулы органических веществ.
1) CH3-CH2-CH2-OH + HBr — CH3-CH2-CH2-Br + H2O
2) CH3-CH2-CH2-Br + КОН(спирт.) [math]\xrightarrow{t^\circ}[/math] CH3-CH=CH2 + H2O + KBr
3) CH3-CH=CH2 + H2O[math]\xrightarrow{H^+}[/math] CH3-CH(OH)-CH3
4) 3CH3-CH(OH)-CH3 + 2KMnO4 [math]\xrightarrow{t^\circ}[/math] 3CH3-CO-CH3 + 2MnO2 + 2KOH + 2H2O
5) CH3-CO-CH3 + H2 [math]\rightarrow[/math] CH3-CH(OH)-CH3
При растворении пероксида лития Li2O2 в тёплой воде выделяется кислород. Определите массовую долю гидроксида лития в растворе, полученном растворением 2,3 г пероксида лития в 62 г воды. Какой максимальный объём углекислого газа (н.у.) может быть поглощён получившейся щёлочью?
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения физических величин).
1) Составлено уравнение реакции пероксида лития с водой, и рассчитано количество вещества пероксида лития:
2Li2O2 + 2Н2O = 4LiOH + O2↑
n(Li2O2) = m / М = 2,3 / 46 = 0,05 моль
2) Рассчитаны количество вещества и масса гидроксида лития и кислорода:
n(LiOH) = 2n(Li2O2) = 0,1 моль
n(O2) = 0,5n(Li2O2) = 0,025 моль
m(LiOH) = 0,1 • 24 = 2,4 г
m(O2) = 0,025 • 32 = 0,8 г
3) Определена масса раствора, и рассчитана массовая доля гидроксида лития в нём:
m(р-ра) = 2,3 + 62 • 0,8 = 63,5 г
w(LiOH) = 2,4 / 63,5 = 0,038 или 3,8%
4) Записано уравнение реакции избытка углекислого газа со щёлочью, и найден объём углекислого газа:
LiOH + СO2 = LiHCO3
n(СO2) = n(LiOH) = 0,1 моль
V(CO2) = 0,1 • 22,4 = 2,24 л
Некоторое органическое соединение содержит 69,6% кислорода по массе. Молярная масса этого соединения в 1,586 раза больше молярной массы воздуха. Известно также, что это вещество способно вступать в реакцию этерификации с пропанолом-2.
На основании данных условия задачи:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества;
3) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции этого вещества с пропанолом-2.
1) Определено число атомов углерода, водорода и кислорода в соединении СxНуОz
M(CxHyOz) = 1,58621 • 29 = 46 г/моль
w(O) = 16 • z / 46 = 0,697
z = 2
M(CxHy) = 46 - 16 • 2 = 46 - 32 = 14 г/моль
x = 1
y = 2
2) Определена молекулярная формула вещества: СН2O2.
3) Составлена структурная формула вещества:
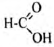
4) Составлено уравнение реакции с пропанолом-2:
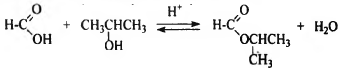
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||