Вариант 13
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
1) Na 2) К 3) F 4) Li 5) Cl
Определите, одновалентные ионы каких из указанных в ряду элементов имеют конфигурацию внешнего электронного слоя 2s22p6. Запишите в поле ответа номера выбранных элементов.
Расположите в порядке увеличения атомного радиуса химические элементы:
1. Na
2. Mg
3. K
1) Na 2) К 3) F 4) Li 5) Cl
Из числа указанных в ряду элементов выберите два элемента, которые в соединениях проявляют отрицательную степень окисления. Запишите в поле ответа номера выбранных элементов.
И ионные, и ковалентные химические связи имеются в веществе:
1. НСl
2. H2SO4
3. NaOH
4. NH4Br
5. С2Н5ОН
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) NH4NO3
Б) СаНРO4
В) Na[Zn(OH)4]
КЛАСС/ГРУППА
1) кислая соль
2) средняя соль
3) основная соль
4) комплексная соль
Из предложенного перечня выберите два вещества, при взаимодействии которых с алюминием образуется соль.
1. Fe
2. Cl2
3. Fe2O3
4. O2
5. S
Из предложенного перечня выберите два оксида, при взаимодействии которых с водой образуется кислота.
1. SiO2
2. SO3
3. BaO
4. P2O5
5. K2O
Гидроксид алюминия реагирует с:
1. H2SO4
2. H2S
3. Ba(NO3)2
4. Sr(OH)2
5. Fe
Задана следующая схема превращений веществ:
[math]Fe\xrightarrow XFe(NO_3)_2\xrightarrow YFe(NO_3)_3[/math]
Определите, какие из указанных веществ являются веществами X и Y.
1. HNO3 (конц.)
2. Cu(NO3)2
3. KNO3
4. NH3
5. Al(NO3)3
Установите соответствие между формулой вещества и степенью окисления азота в нём. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) NF3
Б) H2N2O2
В) NH4HCO3
Г) Ca(NO2)2
СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТА
1) -3
2) +1
3) +2
4) +3
5) +4
6) +5
Установите соответствие между простыми веществами и формулами реагентов, с которыми они могут взаимодействовать.
ПРОСТОЕ ВЕЩЕСТВО
А) Al
Б) Br2
В) S
Г) H2
ФОРМУЛЫ РЕАГЕНТОВ
1) H2SO4(paзб.), Р
2) Н3РO4, СН4
3) С2Н4, O2
4) Сu, N2
5) O2, Аl
6) KI, Сl2
Установите соответствие между формулой углеводорода и его названием.
ФОРМУЛА УГЛЕВОДОРОДА
А) С2Н4
Б) С8Н8
В) С3Н6
Г) С3Н4
НАЗВАНИЕ СОЕДИНЕНИЯ
1) этан
2) бензол
3) стирол
4) этен
5) циклопропан
6) пропадиен
Из предложенного перечня выберите два вещества, которые являются гомологами.
1. бензол
2. стирол
3. этанол
4. толуол
5. этандиол-1,2
Из предложенного перечня выберите два вещества, которые реагируют с хлороводородом.
1. бензол
2. толуол
3. бутан
4. стирол
5. пропин
Из предложенного перечня выберите два вещества, с которыми реагируют и фенол, и глицерин.
1. K
2. Al(OH)3
3. HNO3
4. KHO3
5. HCOOH
Из предложенного перечня выберите два вещества, с которыми реагируют аминокислоты.
1. ароматические углеводороды
2. одноатомные спирты
3. простые эфиры
4. непредельные углеводороды
5. аминокислоты
Задана следующая схема превращений веществ:
ацетилен [math]\xrightarrow X[/math] этаналь [math]\xrightarrow Y[/math] этанол
Определите, какие из указанных веществ являются веществами X и Y.
1. Н2(кат.)
2. H2O2
3. Н2O (Hg2+)
4. КМnO4 (H+)
5. O2 (кат.)
Установите соответствие между углеводородом и продуктом, который преимущественно образуется при его взаимодействии с хлором в соотношении 1:1. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УГЛЕВОДОРОД
А) изобутан
Б) бутен-2
В) бутадиен-1,3
Г) бутан
ПРОДУКТ ХЛОРИРОВАНИЯ
1) 2,3-дихлорбутан
2) 1,4-дихлорбутан
3) 2-метил-2-хлорпропан
4) 1,2-дихлорбутан
5) 1,4-дихлорбутен-2
6) 2-хлорбутан
Установите соответствие между схемой реакции и веществом X, которое является одним из реагентов в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) X + СuО → формальдегид + Сu + Н2О
Б) X + КМnO4(Н+) → ацетон + К+ + Мn+2 + Н2O
В) X + H2SO4 (конц.) → диметиловый эфир + Н2O
Г) X + К → этилат калия + Н2
ВЕЩЕСТВО X
1) муравьиная кислота
2) уксусная кислота
3) метанол
4) этанол
5) пропанол-1
6) пропанол-2
Взаимодействие метана с хлором относится к реакциям:
1. каталитическим
2. обратимым
3. гомогенным
4. присоединения
5. окислительно-восстановительным
Из предложенного перечня выберите два внешних воздействия, которые не влияют на скорость реакции
Мg(тв.) + 2НСl(р-p) = MgCl2(p-p) + Н2(г)↑.
1. повышение температуры
2. добавление хлорида магния
3. измельчение магния
4. увеличение концентрации кислоты
5. увеличение давления
Установите соответствие между названием металла и электролитическим способом его получения.
МЕТАЛЛ
А) калий
Б) медь
В) хром
Г) кальций
СПОСОБ ПОЛУЧЕНИЯ
1) электролиз водного раствора сульфата
2) электролиз расплавленного хлорида
3) электролиз расплавленного нитрата
4) электролиз водного раствора гидроксида
Установите соответствие между формулой соли и средой её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) (СН3СОО)2Ва
Б) Fe(NO3)2
В) Na2SiO3
Г) MgCl2
СРЕДА РАСТВОРА
1) кислая
2) щелочная
3) нейтральная
Установите соответствие между уравнением обратимой химической реакции и одновременным изменением внешних условий, приводящих к смещению химического равновесия в сторону продуктов реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УРАВНЕНИЕ РЕАКЦИИ
А) H2(г) + F2(г) [math]\rightleftarrows[/math] 2HF(г) + Q
Б) H2(г) + I2(тв.) [math]\rightleftarrows[/math] 2HI(г) - Q
В) CO(г) + H2O(г) [math]\rightleftarrows[/math] CO2(г) + H2(г) + Q
Г) C4H10(г) [math]\rightleftarrows[/math] C4H6(г) + 2H2(г) - Q
ИЗМЕНЕНИЕ ВНЕШНИХ УСЛОВИЙ
1) увеличение температуры и концентрации водорода
2) уменьшение температуры и концентрации водорода
3) увеличение температуры и уменьшение концентрации водорода
4) уменьшение температуры и увеличение концентрации водорода
Установите соответствие между формулами веществ и реагентом, с помощью которого можно различить их водные этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛЫ ВЕЩЕСТВ
А) Al(NO3)3 и Ca(NO3)
Б) Na3PO4 и Na2SO4
В) КВr и НСl
Г) KI и NaNO3
РЕАКТИВ
1) AlCl3(p-p)
2) AgNO3
3) Fe
4) KOH(р-р)
5) ВаСl2(р-р)
Установите соответствие между веществом и промышленным способом его получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
МЕТАЛЛ
А) алюминий
Б) железо
В) натрий
Г) литий
СПОСОБ ПОЛУЧЕНИЯ
1) восстановлением углем из оксида
2) электролизом расплава соли
3) вытеснением из расплава соли магнием
4) восстановлением хромом из оксида
5) электролизом расплава оксида в криолите
Из 150 г раствора с массовой долей бромида натрия 6% выпарили 10г воды и добавили 5 г той же соли. Чему равна массовая доля соли в полученном растворе? (Запишите число с точностью до десятых.)
Ответ: _____________ %
В результате реакции, термохимическое уравнение которой
СН4(г) + 2O2(г) = СO2(г) + 2Н2O(г) + 896 кДж
выделилось 1792 кДж теплоты. Определите массу сгоревшего метана. (Запишите число с точностью до целых.)
Ответ:___________________г
Какая масса алюминия потребуется для восстановления 0,4 моль оксида железа(III)? (Запишите число с точностью до десятых.)
Ответ: _____________ г
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции:
К2МnО4 + ... → МnВr2 + Вr2 + ... + Н2О
Определите окислитель и восстановитель.
1) Составлен электронный баланс:
[math]1\;\vert\;Mn^{+6}\;+\;4\overline e\rightarrow Mn^{+2}[/math]
[math]2\;\vert\;2Br^{-1}\;-\;2\overline e\rightarrow Br_2^0[/math]
2) Указано, что бромоводород (за счет брома в степени окисления -1) является восстановителем, а манганат калия (за счет марганца в степени окисления +6) - окислителем.
3) Определены недостающие вещества, и расставлены коэффициенты в уравнении реакции:
K2MnO4 + 8HBr = MnBr2 +2Br2 + 4H2O + 2KBr
Железную окалину растворили в концентрированной азотной кислоте. К полученному раствору добавили раствор гидроксида натрия. Выделившийся осадок отделили и прокалили. Образовавшийся твёрдый остаток сплавили с железом. Напишите уравнения четырёх описанных реакций.
1) Fe3O4 + 10HNO3 = 3Fe(NO3)3 + NO2 + 5H2O
2) Fe(NO3)3 + 3NaOH = 3NaNO3 + Fe(OH)3↓
3) 2Fe(OH)3 = Fe2O3 + 3H2O (при нагревании)
4) Fe2O3 + Fe = 3FeO (при нагревании)
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
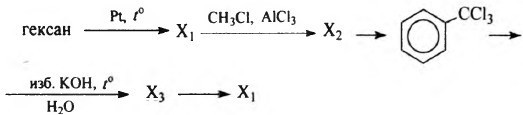
При написании уравнений реакций используйте структурные формулы органических веществ.
Хлорид фосфора(V) массой 4,17 г полностью прореагировал с водой. Какой объём раствора гидроксида калия с массовой долей 10% (плотностью 1,07 г/мл) необходим для полной нейтрализации полученного раствора? В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения физических величин).
1) Записаны уравнения реакций гидролиза хлорида фосфора и нейтрализации двух кислот:
PCl5 + 4H2O = H3PO4 + 5HCl
H3PO4 + 3KOH = K3PO4 + 3H2O
HCl + KOH = KCl + H2O
2) Рассчитаны количество вещества хлорида фосфора(V) и кислот, образовавшихся при гидролизе:
n(PCl5) = 4,17 / 208,5 = 0,02 моль
n(H3PO4) = n(PCl5) = 0,02 моль
n(HCl) = 5n(PCI5) = 0,1 моль
3) Рассчитаны необходимые количество вещества и масса щелочи:
n(KOH) = n(HCl) + 3n(H3PO4) = 0,1 + 0,06 = 0,16 моль
m(KOH) = 0,16 * 56 = 8,96 г
4) Рассчитаны масса и объем раствора щелочи:
m(р-ра)(KOH) = m(KOH) / w(KOH) = 8,96 / 0,10 = 89,6 г
V(р-ра)(KOH) = m(р-ра)(KOH) / р = 8,96 / 1,07 = 83,7 мл.
При сгорании 18,8 г органического вещества получили 26,88 л (н.у.) углекислого газа и 10,8 мл воды. Известно, что это вещество реагирует как с гидроксидом натрия, так и с бромной водой.
На основании данных условия задачи:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу органического вещества;
3) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции данного вещества с бромной водой.
Общая формула вещества - CxHyOz
1) Найдены количество вещества углекислого газа и воды:
n(CO2) = 26,88 / 22,4 =1,2 моль
n(H2O) = 10,8 / 18 = 0,6 моль
2) Определена молекулярная формула вещества:
n(С) = n(СO2) = 1,2 моль
m(C) = 1,2 * 12 = 14,4 г
n(H) = 2n(H2O) = 1,2 моль
m(H) = 1,2 г
m(O) = 18,8 - 14,4 - 1,2 = 3,2 г
n(O) = 3,2 / 16 = 0,2 моль
x : y : z = 1,2 : 1,2 : 0,2 = 6 : 6 : 1
Молекулярная формула - C6H6O
3) Составлена структурная формула вещества:
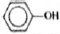
4) Составлено уравнение реакции данного вещества с бромной водой:
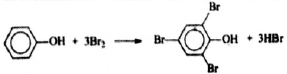
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||