Вариант 5
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
Восьмиэлектронную внешнюю оболочку в основном состоянии имеют частицы:
1. Al3+
2. C2+
3. S2-
4. F
5. Cl5+
Расположите в порядке уменьшения атомного радиуса химические элементы:
1. Al
2. Mg
3. B
Степень окисления (А) и валентность (Б) атомов в молекуле азота равны:
1. 1
2. 2
3. 3
4. 4
5. 0
Молекулярное строение имеют:
1. пропанол-2
2. ацетат калия
3. углекислый газ
4. метилат натрия
5. карбонат кальция
Установите соответствие между формулой вещества и классом, к которому это вещество принадлежит.
ФОРМУЛА ВЕЩЕСТВА
А) NH4HSO4
Б) КСlO4
В) N2O
КЛАСС
1) соль средняя
2) оксид кислотный
3) оксид несолеобразующий
4) соль кислая
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует водород.
1. сера
2. кремний
3. разбавленная азотная кислота
4. гидроксид натрия
5. оксид железа(III)
Из предложенного перечня веществ выберите два вещества, с которыми реагируют и оксид фосфора(V), и оксид натрия.
1. гидроксид бария
2. вода
3. углекислый газ
4. кислород
5. азотная кислота
Гидрокарбонат натрия реагирует в водном растворе с:
1. H2SO4
2. NaOH
3. Zn
4. K2SO4
5. SiO2
В заданной схеме превращений
[math]Fe\xrightarrow XFeCl_3\xrightarrow YFeCl_2[/math]
веществами X и Y соответственно являются:
1. HCl
2. Cl2
3. C
4. Fe
5. H2O
Установите соответствие между схемой реакции и формулой окислителя в ней.
СХЕМА РЕАКЦИИ
А) К2СО3 + Вr2 → КВr + КВrО3 + СО2
Б) Вг2 + CI2 → ВrСl
В) Вr2 + I2 → IBr
Г) HBr + HBrO3 → Вr2 + Н2O
ФОРМУЛА ОКИСЛИТЕЛЯ
1) K2CO3
2) Br2
3) Cl2
5) HBr
6) HBrO3
4) I2
Установите соответствие между исходными веществами и основным продуктом их взаимодействия.
ФОРМУЛЫ ВЕЩЕСТВ
А) Сr(ОН)3 + СsОН(водн. р-р)
Б) Cr(OH)3 + Cs2O 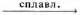
В) Сr(ОН)3 + КОН 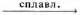
Г) Сr(ОН)3 + К2СO3 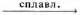
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) CsCrO2
2) Cs3[Cr(OH)6]
3) KCrO2
4) K3[Cr(OH)6]
Установите соответствие между формулой органического соединения и его названием.
ФОРМУЛА СОЕДИНЕНИЯ
А) С2Н5—ОН
Б) С6Н5—СН=СН2
В) СН2(ОН)—СН(ОН)—СН2(ОН)
Г) СН2=С(СН3)—СН=СН2
НАЗВАНИЕ СОЕДИНЕНИЯ
1) дивинил
2) этанол
3) изопрен
4) глицерин
5) толуол
6) стирол
Атомы углерода только в sр3-гибридном состоянии находятся в молекулах
1. стирола
2. глицерина
3. пропанола-2
4. толуола
5. этаналя
Этин, в отличие от этена, реагирует с
1. натрием
2. хлором
3. аммиачным раствором оксида серебра
4. кислородом
5. раствором перманганата калия
Из предложенного перечня веществ выберите два вещества, с которыми реагирует глицерин.
1. гидроксид меди(II)
2. гидроксид меди(I)
3. углекислый газ
4. угарный газ
5. натрий
Из предложенного перечня выберите два вещества, с которыми реагирует аминоуксусная кислота.
1. уксусная кислота
2. аммиак
3. азот
4. изобутан
5. сульфат бария
В заданной схеме превращений
[math]CH_4\xrightarrow XCH_3Br\xrightarrow YCH_3NH_2[/math]
веществами X и Y соответственно являются
1. НВг
2. Вr2
3. N2
4. NH3
5. NH4Br
Установите соответствие между веществом и продуктом его дегидрирования при нагревании с катализатором.
ВЕЩЕСТВО
А) циклогексан
Б) изобутан
В) гептан
Г) гексан
ПРОДУКТ ДЕГИДРИРОВАНИЯ
1) бензол
2) 2-метилпропен
3) циклогептан
4) гексен-2
5) бутадиен-1,2
6) толуол
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) пропанол-1 и оксид меди(II)
Б) пропанол-2 и оксид меди(II)
В) пропанол-2 и муравьиная кислота
Г) пропин и вода
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) пропаналь
2) ацетон
3) пропен
4) изопропанол
5) пропилацетат
6) изопропилформиат
Взаимодействие раствора гидроксида натрия с азотной кислотой относится к реакциям:
1. каталитическим
2. гомогенным
3. экзотермическим
4. окислительно-восстановительным
5. замещения
Скорость реакции Fe + 2НСl(р-р) = FeCl2 + Н2 увеличится при
1. добавлении ингибитора
2. нагревании
3. увеличении концентрации FeCl2
4. увеличении давления в системе
5. увеличении концентрации кислоты
Установите соответствие между формулой вещества и продуктом, выделяющимся на катоде при электролизе водного раствора этого вещества.
ФОРМУЛА ВЕЩЕСТВА
А) NaNO3
Б) Cu(NO3)2
В) RbHCO3
Г) SnCl2
КАТОДНЫЙ ПРОДУКТ
1) кислород
2) только металл
3) только водород
4) металл и водород
5) азот
6) хлор
Установите соответствие между названием соли и средой ее водного раствора.
НАЗВАНИЕ СОЛИ
А) гидросульфид калия
Б) гидросульфит натрия
В) ортофосфат калия
Г) хлорид хрома(III)
СРЕДА РАСТВОРА
1) нейтральная
2) кислая
3) щелочная
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при уменьшении давления в системе:
УРАВНЕНИЕ РЕАКЦИИ
А) SO2Cl2(г) [math]\rightleftarrows[/math] SO2(г) + Cl2(г)
Б) 2H2(г) + O2(г) [math]\rightleftarrows[/math] 2H2O(г)
В) 2HCl(г) [math]\rightleftarrows[/math] H2(г) + Cl2(г)
Г) N2(г) + 3H2(г) [math]\rightleftarrows[/math] 2NH3(г)
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) в сторону продуктов реакции
2) в сторону исходных веществ
3) практически не смещается
Установите соответствие между реагирующими веществами и реагентом, с помощью которого их можно отличить друг от друга.
ВЕЩЕСТВА
А) этаналь и ацетон
Б) пропанол-1 и этиленгликоль
В) метиламин и пропан
Г) этанол и глицерин
РЕАГЕНТ
1) метилоранж (р-р)
2) Сu(ОН)2
3) Fe(OH)3
4) H2SO4 (р-р)
5) КСl
В качестве мономеров для синтеза высокомолекулярных соединений используют:
1. пропен
2. бутин-1
3. толуол
4. бутадиен-1,3
5. пентадиен-1,4
К 250 г 10%-ного раствора нитрата натрия добавили 10 г этой же соли и 50 мл воды. Чему равна массовая доля нитрата натрия в полученном растворе? (Запишите число с точностью до десятых.)
Ответ: ___________________%.
В результате реакции, термохимическое уравнение которой
2Н2(г) + О2(г) = 2Н2O(г) + 484 кДж,
выделилось 968 кДж теплоты. Вычислите массу образовавшейся при этом воды. (Запишите число с точностью до целых).
Ответ: ___________________г.
Рассчитайте массу кислорода, необходимого для полного сжигания 2,24 л (н.у.) угарного газа. (Запишите число с точностью до десятых.)
Ответ: ___________________г.
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции:
Na2SO3 + ... H2SO4 → ... + MnSO4 + K2SO4 + H2O
Определите окислитель и восстановитель.
Элементы ответа:
1) Составлен электронный баланс:
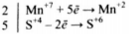
2) Указано, что Na2SO3 (за счет серы в степени окисления +4) является восстановителем, а KMnO4 (за счет марганца в степени окисления +7) - окислителем.
3) Определены недостающие вещества, и расставлены коэффициенты в уравнении реакции:
5Na2SO3 + 2KMnO4 + 3H2SO4 = 5Na2SO4 + 2MnSO4 + K2SO4 + 3H2O
Натрий сожгли на воздухе. Образовавшееся вещество обработали хлороводородом. Полученное простое вещество при нагревании вступило в реакцию с оксидом хрома(III) в присутствии гидроксида калия. При обработке раствора одной из образовавшихся солей хлоридом бария выпал жёлтый осадок. Напишите уравнения четырёх описанных реакций.
1) [math]2Na+O_2=Na_2O_2[/math]
2) [math]Na_2O_2+4HCl=2NaCl+Cl_2+2H_2O[/math]
3) [math]Cr_2O_3+3Cl_2+10KOH\xrightarrow{t^\circ}2K_2CrO_4+6KCl+5H_2O[/math]
4) [math]K_2CrO_4+BaCl_2=BaCrO_4\downarrow+2KCl[/math]
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
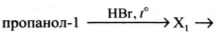
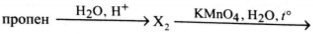
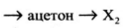
При написании уравнений реакций используйте структурные формулы органических веществ
1) [math]CH_3-CH_2-CH_2-OH+HBr\rightarrow CH_3-CH_2-CH_2-Br+H_2O[/math]
2) [math]CH_3-CH_2-CH_2-Br+KOH\xrightarrow{t^\circ}CH_3-CH=CH_2+H_2O+KBr[/math]
3) [math]CH_3-CH=CH_2+H_2O\xrightarrow{H^+}CH_3-CH(OH)-CH_3[/math]
4) [math]\begin{array}{l}3CH_3-CH(OH)-CH_3+2KMnO_4\xrightarrow{t^\circ}3CH_3-CO-CH_3+\\+2MnO_2+2KOH+2H_2O\end{array}[/math]
5) [math]CH_3-CO-CH_3+H_2\rightarrow CH_3-CH(OH)-CH_3[/math]
При растворении пероксида лития Li2O2 в теплой воде выделяется кислород. Определите массовую долю гидроксида лития в растворе, полученном растворением 2,3 г пероксида лития в 62 г воды. Какой максимальный объем углекислого газа (н.у.) может быть поглощен получившейся щелочью?
Элементы ответа:
1) Составлено уравнение реакции пероксида лития с водой, и рассчитано количество вещества пероксида лития:
2Li2O2 + 2H2O = 4LiOH + O2 ↑
m(Li2O2) = m / M = 2,3 / 46 = 0,05 моль
2) Рассчитаны количество вещества и масса гидроксида лития и кислорода:
n(LiOH) = 2n(Li2O2) = 0,1 моль
n(O2) = 0,5n(Li2O2) = 0,025 моль
m(LiOH) = 0,1 x 24 = 2,4 г
m(O2) = 0,025 x 32 = 0,8 г
3) Определена масса раствора, и рассчитана массовая доля гидроксида лития в нем:
m(p-pa) = 2,3 + 62 - 0,8 = 63,5 г
ω(LiOH) = 2,4 / 63,5 = 0,038 или 3,8%
4) Записано уравнение реакции избытка углекислого газа со щелочью, и найден объем углекислого газа:
LiOH + CO2 = LiHCO3
n(CO2) = n(LiOH) = 0,1 моль
V(CO2) = 0,1 x 22,4 = 2,24 л
Некоторое органическое соединение содержит 69,6% кислорода по массе. Молярная масса этого соединения в 1,586 раза больше молярной массы воздуха. Известно также, это вещество способно вступать в реакцию этерификации с пропанолом-2.
На основании данных условия задачи:
1. произведите вычисления, необходимые для установления молекулярной формул органического вещества;
2. запишите молекулярную формулу органического вещества;
3. составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4. напишите уравнение реакции этого вещества с пропанолом-2.
Элементы ответа:
1) Определено число атомов углерода, водорода и кислорода в соединении CxHyOz:
M(CxHyOz) = 1,58621 x 29 = 46 г/моль
w(O) = 16 x z / 46 = 0,697
z = 2
M(CxHy) = 46 - 16 x 2 = 46 -32 = 14 г/моль
х = 1
у = 2
2) Определена молекулярная формула вещества CH2O2
3) Составлена структурная формула вещества:
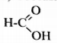
4) Составлено уравнение реакции с пропанолом-2:
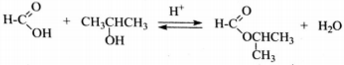
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||