Вариант 6
Часть 1.
Ответом к заданиям 1–5, 7–10, 12–17 является одна цифра, которая соответствует номеру правильного ответа. Для вашего удобства данные задания оснастили радио-кнопками. Работать со смартфона будет проще. Ответом к заданию 6 являются три цифры, которые соответствуют номерам правильных ответов. Запишите эти цифры в поле ответа в тексте работы. Ответом к заданиям 11 и 18 являются две цифры, которые соответствуют номерам правильных ответов. ответом к заданиям 24–26 является число. Запишите полученное число с указанной степенью точности в поле ответа.
Электронная конфигурация Is2 соответствует частице
1. H
2. H+
3. H-
4. He2+
Верны ли следующие суждения о железе и его соединениях?
А. Железо находится в VIIIА группе.
Б. Наиболее типичная степень окисления железа +8.
1. верно только А
2. верно только Б
3. верны оба суждения
4. оба суждения неверны
Веществом с ковалентной полярной связью является
1. водород
2. бром
3. кислород
4. вода
Степень окисления +3 атом хлора имеет в соединении
1. СlO3
2. Cl2O6
3. Ba(ClO2)2
4. KClO3
Немолекулярное строение имеет
1. железо
2. водород
3. кислород
4. угарный газ
В перечне веществ к кислотным оксидам относятся вещества
1. CO2
2. Fe2O3
3. Fe3O4
4. CaO
5. Cl2O7
6. CrO3
Общим свойством меди и цинка является их способность взаимодействовать с
1. раствором КОН
2. раствором ВаСl2
3. раствором HNO3
4. разбавленной H2SO4
Оксид фосфора (V) не взаимодействует с:
1. водой
2. хлоридом натрия
3. гидроксидом калия
4. оксидом кальция
Верны ли следующие суждения о серной кислоте?
А. Концентрированная серная кислота относится к водоотнимающим реагентам.
Б. Разбавленная серная кислота растворяет медь, но не растворяет серебро.
1. верно только А
2. верно только Б
3. верны оба суждения
4. оба суждения неверны
Гидрокарбонаты в растворе переходят в карбонаты при действии на них
1. любой соли
2. любой кислоты
3. любого оксида
4. любой щелочи
В схеме превращений
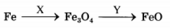
веществами X и Y соответственно являются:
1. HNO3
2. O2
3. H2
4. CO2
5. H2SO4
Изомером циклогексана является
1. 3-метилгексан
2. циклопентан
3. бензол
4. гексен-2
Для какого углеводорода особенности химических свойств объясняются единой π-электронной системой в молекуле?
1. циклобутан
2. бутен-1
3. метилциклогексан
4. бензол
Фенол образует белый осадок при взаимодействии с
1. бромной водой
2. азотной кислотой
3. гидроксидом калия
4. аммиаком
Верны ли следующие суждения о жирах?
А. Все жиры твёрдые при обычных условиях вещества.
Б. С химической точки зрения жиры относятся к сложным эфирам
1. верно только А
2. верно только Б
3. верны оба суждения
4. оба суждения неверны
Сложный эфир образуется при реакции этанола с
1. метанолом
2. глицином
3. пропином
4. натрием
Аминоуксусная кислота реагирует с
1. соляной кислотой
2. метаном
3. углекислым газом
4. оксидом кремния
В схеме превращений
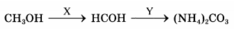
веществами X и Y соответственно являются:
1. CuO
2. Cu(OH)2
3. NH3
4. CO2
5. Ag2O (NH3 * H2O)
К экзотермическим реакциям относится взаимодействие
1. азота с кислородом
2. углерода с углекислым газом
3. воды с углеродом
4. пропена с бромом
Скорость реакции цинка с раствором серной кислоты не зависит от
1. числа взятых гранул цинка
2. степени измельчения цинка
3. концентрации серной кислоты
4. температуры
Слабым и сильным электролитами являются соответственно вещества:
1. уксусная кислота и этилацетат
2. бромоводород и этанол
3. пропанол и ацетон
4. пропионовая кислота и ацетат натрия
Верны ли следующие суждения о правилах работы в лаборатории?
А. В лаборатории нельзя знакомиться с запахом веществ.
Б. Все соли натрия и калия даже в умеренных дозах ядовиты для человека.
1. верно только А
2. верно только Б
3. верны оба суждения
4. оба суждения неверны
Промышленное получение аммиака основано на реакции, схема которой:
1. Ca(OH)2 + NH4Cl →
2. Mg3N2 + H2O →
3. H2 + N2 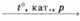
4. NH4Cl 
Чему равна массовая доля соли в растворе, полученном при смешивании 1 кг 11%-ного раствора с 3 кг 15%-ного раствора этой соли?
Ответ: _________ %.
(Запишите число с точностью до целых.)
Какой объём газа (н.у.) не вступит в реакцию, если сжигать 50 л водорода в 50 л кислорода?
Ответ: _________ л.
(Запишите число с точностью до целых.)
Рассчитайте объём (н.у.) ацетилена, который выделится при взаимодействии с водой 50 г карбида кальция, содержащего 8% примесей.
Ответ: _________ л.
(Запишите число с точностью до десятых.)
В заданиях 27–35 к каждому элементу подберите соответствующий элемент и запишите выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между названием неорганического соединения и классом, к которому оно принадлежит.
НАЗВАНИЕ СОЕДИНЕНИЯ
А) угарный газ
Б) мрамор
В) пищевая сода
Г) гашеная известь
КЛАСС СОЕДИНЕНИЙ
1) средние соли
2) кислые соли
3) основные соли
4) оксиды
5) основания
6) кислотные основания
Установите соответствие между формулой соли и степенью окисления хрома в ней.
ФОРМУЛА СОЛИ
А) K2CrO4
Б) CaCr2O7
В) CrO2P2
Г) Ba3[Cr(OH)6]2
СТЕПЕНЬ ОКИСЛЕНИЯ ХРОМА
1) 0
2) +2
3) +3
4) +4
5) +5
6) +6
Установите соответствие между формулой вещества и продуктом, выделяющимся на катоде при электролизе водного раствора этого вещества.
ФОРМУЛА ВЕЩЕСТВА
А) NaNO3
Б) Cu(NO3)2
В) RbHCO3
Г) SnCl2
КАТОДНЫЙ ПРОДУКТ
1) кислорода
2) только металл
3) только водород
4) металл и водород
5) азот
6) хлор
Установите соответствие между названием соли и способностью ее к гидролизу.
НАЗВАНИЕ СОЛИ
А) сульфид цезия
Б) нитрат бария
В) сульфат натрия
Г) карбонат аммония
СПОСОБНОСТЬ К ГИДРОЛИЗУ
1) гидролизу не подвергается
2) гидролизуется по катиону
3) гидролизуется по аниону
4) гидролизуется по катиону и аниону
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при уменьшении давления в системе:
ФОРМУЛЫ ВЕЩЕСТВ
А) SO2Cl2(г) 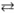 SO2(г) + Cl2(г)
SO2(г) + Cl2(г)
Б) 2SO2(г) + O2(г)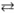 2SO2(г)
2SO2(г)
В) 2HI(г)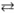 H2(г) + I2(тв)
H2(г) + I2(тв)
Г) S(г) + H2(г)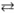 H2S(г)
H2S(г)
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) в сторону продуктов реакции
2) в сторону исходных веществ
3) практически не смещается
Установите соответствие между исходными веществами и основным продуктом их взаимодействия.
ФОРМУЛЫ ВЕЩЕСТВ
А) Al(OH)3 + RbOH(водн. р-р)
Б) Al(OH)3 + Rb2O 
В) Al(OH)3 + CsOH
Г) Al(OH)3 + Cs2CO3
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) RbAlO2
2) Rb3[Al(OH)6]
3) CsAlO2
4) Cs3[Al(OH)6]
Установите соответствие между реагирующими веществами и признаками протекающей между ними реакции.
ВЕЩЕСТВА
А) HCl + Na2CO3
Б) CaCl2 + Na2CO3
В) Ca(HCO3)2 + Ca(OH)2
Г) Ca(HCO3)2 + NaOH
ПРИЗНАКИ РЕАКЦИИ
1) выделение бесцветного газа
2) образование черного осадка
3) образование белого осадка
4) изменение окраски раствора
5) видимых признаков не наблюдается
Установите соответствие между реагирующими веществами и органическим продуктом, который преимущественно образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) бензол и хлор (AlCl3)
Б) циклопропан и водород
В) бензол и хлор (УФ)
Г) толуол и водород
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) пропен
2) пропан
3) хлорбензол
4) гексахлорциклогексан
5) ксилол
6) метилциклогексан
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) CH3COONa и NaOH
Б) CH3COOH и CH3OH
В) CH3OH и K
Г) CH3OH и H2SO4
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) Ацетат натрия
2) метил ацетат
3) метилат калия
4) метан
5) диметиловый эфир
6) метаналь
Часть 2.
Запишите сначала номер задания (36, 37 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции
КМnO4 + HBr → МnВr2 + Вr2 + ... + ....
Определите окислитель и восстановитель.
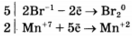
2KMNO4 + 16HBr = 2KBr + 2MnBr2 + 5Br2 + 8H2O
Бром в степени окисления -1 является восстановителем, а марганец +7 (или перманганат калия за счет марганца +7) - окислителем.
Нитрат калия нагрели с порошкообразным свинцом до прекращения реакции. Смесь продуктов обработали водой, а затем полученный раствор профильтровали. Фильтрат подкислили серной кислотой и обработали иодидом калия. Выделившееся простое вещество нагрели с концентрированной азотной кислотой. В атмосфере образовавшегося при этом бурого газа сожгли красный фосфор.
Запишите уравнения описанных реакций.
1) KNO3 + Pb 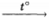 KNO2 + PbO
KNO2 + PbO
2) 2KNO2 + 2H2SO4 + 2KI = 2K2SO4 + 2NO↑ + I2 + 2H2O
3) I2 + 10HNO3 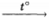 2HIO3 + 10NO2↑ + 4H2O
2HIO3 + 10NO2↑ + 4H2O
4) 10NO2 + 8P = 4P2O5 + 5N2
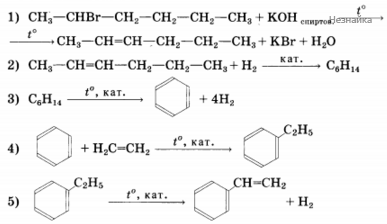
Напишите уравнение реакций, с помощью которых можно осуществить следующие превращения:
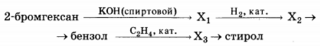
При написании уравнений реакций используйте структурные формулы органических соединений.
Смесь железных и серебряных опилок обработали избытком разбавленной соляной кислоты, при этом выделилось 4,48 л (н.у.) водорода. Какой объём 20%-ной серной кислоты плотностью 1,14 г/мл понадобился бы для растворения всего железа, содержащегося в исходной смеси?
Vр-ра(H2SO4) = 86 мл
Некоторое органическое соединение, помимо углерода и водорода, содержит азот, массовая доля которого 23,7%.. Это соединение обладает нециклическим строением, взаимодействует с соляной кислотой с образованием соли, молекула его содержит два углеводородных радикала. На основании этих данных:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу исходного органического вещества;
3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) приведите уравнение реакции его взаимодействия с соляной кислотой.
2) молекулярная формула C3H9N
3) структурная формула
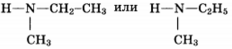
4) уравнение реакции (CH3)(C2H5)NH + HCl → (CH3)(C2H4)NH2+ Cl-
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||