Вариант 4
Часть 1.
Ответом к заданиям 1–5, 7–10, 12–17 является одна цифра, которая соответствует номеру правильного ответа. Для вашего удобства данные задания оснастили радио-кнопками. Работать со смартфона будет проще. Ответом к заданию 6 являются три цифры, которые соответствуют номерам правильных ответов. Запишите эти цифры в поле ответа в тексте работы. Ответом к заданиям 11 и 18 являются две цифры, которые соответствуют номерам правильных ответов. ответом к заданиям 24–26 является число. Запишите полученное число с указанной степенью точности в поле ответа.
Такую же электронную конфигурацию как ион S2- имеет частица
1. O2-
2. Ca2+
3. Si4+
4. Al3+
В ряду элементов
Be → B → C → N1. уменьшается число электронных слоёв в атомах
2. уменьшается число электронов на внешнем энергетическом уровне атома
3. возрастают радиусы атомов
4. усиливаются неметаллические свойства
Водородные связи образуются между молекулами
1. этанола
2. ацетальдегида
3. этилацетата
4. этана
Степень окисления +7 иод имеет в соединении
1. Ba5(IO6)2
2. I2O5
3. Ca(IO3)2
4. KIO
Металлическую кристаллическую решётку имеет
1. мел
2. иод
3. калий
4. глюкоза
Среди перечисленных веществ к классу кислот относятся:
1. H3P
2. HF
3. HMnO4
4. NaHCO3
5. HCOOH
6. CH3COOK
Фосфор вступает в реакцию с
1. оксидом магния
2. калием
3. гидроксидом алюминия
4. водородом
Между собой не взаимодействуют
1. CO2 и Ca(OH)2
2. HCl и Al
3. Zn(OH)2 и NaOH
4. CaO и BaO
Гидроксид железа(III) при обычных условиях взаимодействует с
1. карбонатом натрия
2. кремниевой кислотой
3. гидроксидом меди(II)
4. уксусной кислотой
Для вытеснения олова из водного раствора его соли можно использовать каждый из двух металлов:
1. медь и алюминий
2. натрий и свинец
3. хром и железо
4. кальций и серебро
В схеме превращений
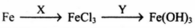
веществами Х и Y являются соответственно:
1. HCl
2. Ca(OH)2
3. H2O
4. Cl2
5. BaCl2
В молекуле какого вещества атом углерода связан двойной связью с атомом кислорода?
1. диметилового эфира
2. бутанола-2
3. глицерина
4. ацетона
С толуолом взаимодействует каждое из двух веществ:
1. CH4 и HNO3
2. H2O и CH3Cl
3. H2 и Cl2
4. HCl и H2SO4
И фенол, и метанол взаимодействуют с
1. литием
2. гидроксидом меди(II)
3. бромной водой
4. оксидом меди(II)
Сложный эфир образуется при взаимодействии пропионовой кислоты с
1. карбонатом натрия
2. бутанолом-2
3. ацетоном
4. гидроксидом натрия
При действий водного раствора щёлочи на 1,2-дибромэтан образуется
1. этанол
2. этиленгликоль
3. этилен
4. ацетилен
Этиламин взаимодействует с
1. соляной кислотой
2. оксидом магния
3. хлоридом натрия
4. гидроксидом натрия
В схеме превращений
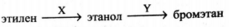
веществами X и Y являются соответственно
1. KOH
2. HBr
3. Br2
4. H2O
5. NaBr
Взаимодействие этана и этина с хлором относится соответственно к реакциям
1. замещения и присоединения
2. замещения и обмена
3. обмена и замещения
4. обмена и присоединения
На скорость реакции
Na2SO3(p-p) + 2HCl(p-p) = 2NaCl(p-p) + SO2↑ + H2O
не влияет изменение
1. концентрации соляной кислоты
2. давления
3. температуры
4. концентрации сульфита натрия
Сокращённому ионному уравнению
Fe3+ + 3OH- = Fe(OH)3
соответствует взаимодействие
1. FeCl2 и NaOH
2. Fe и NaOH
3. Fe2O3 и NaOH
4. FeCl3 и NaOH
Нетоксичным для человека является каждое из двух веществ:
1. Н2 и С6Н5ОН
2. СО и NH3
3. O2 и N2
4. Сl2 и H2S
Верны ли следующие суждения о производстве серной кислоты?
А. Промежуточной стадией производства серной кислоты является каталитическое окисление сернистого газа кислородом при температуре 450 °С.
Б. Сырьём для получения серной кислоты является пирит FeS2.
1. верно только А
2. верно только Б
3. верны оба суждения
4. оба суждения неверны
Смешали 160 г раствора с массовой долей нитрата кальция 15% и 40 г раствора с массовой долей этой же соли 20%. Масса соли в полученном растворе равна _______ г.
(Запишите число с точностью до целых.)При полном окислении 1 г глюкозы С6Н12О6 выделяется 17,6 кДж теплоты. При окислений 1 моль глюкозы выделяется теплота количеством ________ кДж.
(Запишите число с точностью до целых.)
Сульфид железа(II) массой 33,4 г обработали избытком хлороводородной кислоты. Объём (н.у.) газа, выделившегося в результате этой реакции равен _______ л.
(Запишите число с точностью до десятых.)
В заданиях 27–35 к каждому элементу подберите соответствующий элемент и запишите выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между формулой вещества и его принадлежностью к определенному(-ой) классу (группе) органических соединений.
ФОРМУЛА ВЕЩЕСТВА
А) CH3CH2CH2OH
Б) CH3COCH3
В) C10H22
Г) CH2=C(CH3)-CH=CH2
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1) алкадиены
2) кетоны
3) спирты
4) алканы
5) карбоновые кислоты
6) арены
Установите соответствие между изменением степени окисления азота и схемой реакции, в которой это изменением происходит.
ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ
А) N+5 → N+4
Б) N+5 → N+1
В) N+5 → N+2
Г) N-3 → N+2
СХЕМА РЕАКЦИИ
1) Cu + HNO3(разб.) → Cu(NO3)2 + NO + H2O
2) NH3 + O2 → (кат.) NO + H2O
3) Cu + HNO3(конц.) → Cu(NO3)2 + NO2 + H2O
4) HNO3 + CaCO3 → Ca(NO3)2 + CO2 + H2O
5) Mg + HNO3(разб.) → Mg(NO3)2 + N2O + H2O
Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе водного раствора этой соли.
ФОРМУЛА СОЛИ
А) Al(NO3)3
Б) LiCl
В) Cu(NO3)2
Г) NaF
ПРОДУКТ НА АНОДЕ
1) H2
2) O2
3) N2
4) F2
5) Cl2
6) HCl
Установите соответствие между названием соли и отношением этой соли к гидролизу.
НАЗВАНИЕ СОЛИ
А) сульфат аммония
Б) нитрат натрия
В) ацетат магния
Г) фосфат натрия
ОТНОШЕНИЕ К ГИДРОЛИЗУ
1) гидролиз по катиону
2) гидролиз по аниону
3) гидролиз по катиону и аниону
4) гидролизу не подвергается
Установите соответствие между фактором, действующим на равновесную систему

и направлением смещения химического равновесия в этой системе.
ФАКТОР
А) добавление метанола
Б) повышение давления
В) повышение концентрации эфира
Г) добавление гидроксида натрия
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) смещается в сторону продуктов реакции
2) смещается в сторону исходных веществ
3) смещение равновесия не происходит
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать.
ФОРМУЛА ВЕЩЕСТВА
А) Cl2
Б) Al2O3
В) Ca(OH)2
Г) NaHSO3
РЕАГЕНТЫ
1) NaOH, NaCl, HF
2) H2SO4, NaOH, HBr
3) NaHSO4, Br2, SO2
4) NaBr, Ba(OH)2, Fe
5) C6H6, HCl, NaOH
Установите соответствие между формулами двух веществ и реактивом, с помощью которого можно различить эти вещества.
ФОРМУЛЫ ВЕЩЕСТВ
А) HCl (г) NH3
Б) HNO3 и HCl
В) Na2SO4 и KNO3
Г) AlCl3 и MgCl2
РЕАКТИВ
1) NaOH (p-p)
2) Ba(NO3)2 (p-p)
3) CaSO4
4) Cu
5) лакмус
Установите соответствие между углеводородом и продуктом, который преимущественно образуется при его взаимодействии с бромом в соотношении 1:1.
УГЛЕВОДОРОД
А) пропен
Б) пропин
В) циклопропан
Г) 2-метилпропан
ПРОДУКТ РЕАКЦИИ
1) 2-метил-2-бромпропан
2) 1,2-дибромпропан
3) 2-бромпропан
4) 1,3-дибромпропан
5) 1,2-дибромпропен
6) 2,2-дибпромпропан
Установите соответствие между веществом и углеродсодержащими продуктом реакции, который преимущественно образуется при взаимодействии этого вещества с оксидом меди (II).
ВЕЩЕСТВО
А) уксусная кислота
Б) этанол
В) метанол
Г) пропанол-2
ПРОДУКТ РЕАКЦИИ
1) ацетон
2) ацетальдегид
3) формальдегид
4) пропаналь
5) формиат меди(II)
6) ацетат меди(II)
Часть 2.
Запишите сначала номер задания (36, 37 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение
Cr2(SO4)3 + Cl2 + ... → K2CrO4 + KCl + ... H2O
Определите окислитель и восстановитель.
Элементы ответа:
Карбид алюминия полностью растворили в бромоводородной кислоте.
К полученному раствору добавили раствор сульфита калия, при этом наблюдали образование белого осадка и выделение бесцветного газа. Газ поглотили раствором дихромата калия в присутствии серной кислоты. Образовавшуюся соль хрома выделили и добавили к раствору нитрата бария, наблюдали выделение осадка.
Напишите уравнения четырёх описанных реакций.

Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:

При написании уравнений реакций используйте структурные формулы органических веществ.
Газ, выделившийся при взаимодействии 7,4 г нитрида кальция с 9 г воды, полностью поглощён 200 мл 3,5%-ного раствора соляной кислоты (р = 1,05 г/мл). Определите массовую долю хлорида аммония в образовавшемся растворе.
Элементы ответа:
При сгорании 4,48 л (н.у.) газообразного органического вещества получили 35,2 г углекислого газа и 10,8 мл воды. Плотность этого вещества составляет 2,41 г/л (н.у.). Известно также, что это вещество не реагирует с аммиачным раствором оксида серебра, а при реакции его с избытком бромной воды происходит присоединение атомов брома только ко вторичным атомам углерода.
На основании данных условия задачи:
1. произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2. запишите молекулярную формулу органического вещества;
3. составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4. напишите уравнение реакции этого вещества с избытком бромной воды.
Элементы ответа:
Общая формула вещества - CxHyOz
1) Найдены количество вещества углекислого газа, воды и органического вещества:
n(CO2) = 35,2 / 44 = 0,8 моль
m(H2O) = 10,8 / 18 = 0,6 моль
M(CxHyOz) = 2,41 x 22,4 = 54 г/моль
n(CxHyOz) = 4,48 / 22,4 = 0,2 моль
2) Определена молекулярная формула вещества:
n(C) = n(CO2) = 0,8 моль
n(H) = 2n(H2) = 1,2 моль
x = n(C) / n(CxHyOz) = 0,8 / 0,2 = 4
y = n(H) / n(CxHyOz) = 1,2 / 0,2 = 6
4 x 12 + 6 + z x 16 = 30
z = 0
Молекулярная формула C4H6
3) Составлена структурная формула вещества:
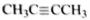
4) Составлено уравнение реакции этого вещества с избытком бромной воды:
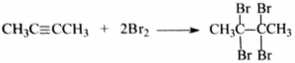
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||