Вариант 1
Часть 1.
Ответом к заданиям 1–5, 7–10, 12–17 является одна цифра, которая соответствует номеру правильного ответа. Для вашего удобства данные задания оснастили радио-кнопками. Работать со смартфона будет проще. Ответом к заданию 6 являются три цифры, которые соответствуют номерам правильных ответов. Запишите эти цифры в поле ответа в тексте работы. Ответом к заданиям 11 и 18 являются две цифры, которые соответствуют номерам правильных ответов. ответом к заданиям 24–26 является число. Запишите полученное число с указанной степенью точности в поле ответа.
Какую электронную конфигурацию имеет атом фтора?
1. 1s22s22p5
2. 1s22s22p4
3. 1s22s22p6
4. 1s22s22p2
В каком ряду химические элементы расположены в порядке увеличения радиуса их атомов?
1. Li → Be → B
2. Sb → As → P
3. N → P → As
4. P → S → Cl
Ионную связь имеет каждое из двух веществ:
1. Na и HF
2. MgCl2 и BaF2
3. H2 и HCl
4. NH3 и H2O2
В каком из перечисленных соединений фосфор проявляется максимальную степень окисления?
1. PBr3
2. P4O6
3. K2HPO4
4. Mg3P2
Молекулярное строение имеет каждое из двух веществ:
1. Fe и Na2SO3
2. Cl2 и NO2
3. CaO и SO2
4. NH3 и Na2CO3
Среди перечисленных веществ к солям относятся:
1. NH4Br
2. SCl2
3. CH3COONa
4. Al(OH)3
5. Na3[Cr(OH)6]
6. Fe2O3
Между какими веществами не протекает химическая реакция?
1. хлором и иодидом натрия
2. фтором и гидроксидом натрия
3. бромом и сероводородом
4. бромом и фтороводородом
Оксид кремния (IV) реагирует с
1. гидроксидом бария
2. кислородом
3. водой
4. азотной кислотой
Как с кислотами, так и со щелочами взаимодействует каждое из двух веществ:
1. оксид меди (II) и гидроксид железа (III)
2. гидроксид цинка и гидрокарбонат натрия
3. оксид алюминия и оксид магния
4. хлорид железа (III) и серная кислота
При термическом разложении какой из указанных солей не образуется твердый остаток?
1. CaCO3
2. (NH4)2CO3
3. AgNO3
4. NaHCO3
В схеме превращений
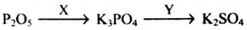
веществами X и Y соответственно являются
1. дихромат калия
2. сульфат магния
3. сульфат натрия
4. гидроксид калия
5. оксид серы (IV)
Изомером пропанола-2 является
1. пропаналь
2. метилэтиловый эфир
3. бутанол-2
4. пропановая кислота
В реакция присоединения с хлором не вступает
1. этилен
2. ацетилен
3. бутан
4. бензол
Фенол не взаимодействует с
1. FeCl3
2. HNO3
3. H2O
4. HCHO
Какое из веществ проявляет как свойства кислот, так и свойства альдегидов?
1. C3H7COOH
2. C7H15COOH
3. C5H9COOH
4. HCOOH
Пентановая кислота образуется в результате взаимодействия
1. пентена-1 с соляной кислотой
2. пентана с азотной кислотой
3. пентанола-1 с гидроксидом натрия
4. пентаналя с гидроксидом меди(II)
Фениламин образует соль при взаимодействии с
1. кислородом
2. хлором
3. водой
4. хлороводородом
В схеме превращений
глюкоза → Х → Y → этан
веществами X и Y являются
1. C2H4
2. C2H5Br
3. C2H5OH
4. CH3–O–CH3
5. C2H2
Взаимодействие воды с барием относится к реакциям
1. замещения, эндотермическим
2. обмена, экзотермическим
3. соединения, экзотермическим
4. замещения, экзотермическим
Верны ли следующие суждения о скорости химической реакции?
А. Взаимодействие цинка с соляной кислотой протекает с большей скоростью, чем с ортофосфорной кислотой той же концентрации.
Б. Скорость реакции в растворе зависит от объема сосуда, в котором проводят реакцию.
1. Верно только А
2. Верно только Б
3. верны оба суждения
4. оба суждения неверны
Реакция ионного обмена с выпадением осадка и образованием воды происходит между растворами
1. гидроксида магния и соляной кислоты
2. серной кислоты и гидроксида бария
3. карбоната натрия и азотной кислоты
4. хлорида железа(II) и гидроксида лития
Реактивом на многоатомные спирты является
1. азотная кислота
2. свежеполученный гидроксид меди(II)
3. аммиачный раствор оксида серебра(I)
4. бромная вода
Синтез аммиака проводят
1. в присутствии катализатора
2. в "кипящем слое"
3. при комнатной температуре
4. при атмосферном давлении
Смешали 400 г раствора с массовой долей азотной кислоты 25% и 200 г раствора с массовой долей этой кислоты 20%. Массовая доля кислоты в полученном растворе равна ______ %. (Запишите число с точностью до десятых).
В результате реакции, термохимическое уравнение которой
C6H12O6(тв.) + 6O2(г) = 6CO2(г) + 6H2O(г) + 2800 кДж,
выделилось 560 кДж теплоты. Количество вещества кислорода, вступившего в реакцию, равно _____ моль. (Запишите число с точностью до десятых).
Объем (н.у) газа, выделившегося при растворении 44 г сульфида железа(II) в избытке соляной кислоты, равен ______ л. (Запишите число с точностью до десятых).
В заданиях 27–35 к каждому элементу подберите соответствующий элемент и запишите выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
Установите соответствие между названием органического вещества и его принадлежностью к определенному(-ой) классу (группе) органических соединений.
НАЗВАНИЕ ВЕЩЕСТВА
А) толуол
Б) бензол
В) метиламин
Г) циклогексан
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1) кислородосодержащее соединение
2) азотосодержащее соединение
3) углеводород
4) галогенопроизводное углеводорода
5) углевод
Установите соответствие между названием элемента и характерными степенями окисления, которые он может проявлять.
НАЗВАНИЕ ЭЛЕМЕНТА
А) кислород
Б) бром
В) кремний
Г) железо
ХАРАКТЕРНЫЕ СТЕПЕНИ ОКИСЛЕНИЯ
1) –4, 0, +2, +4
2) 0, +2, +3, +6
3) –2, –1, 0, +2
4) 0, +2, +4, +6, +7
5) –1, 0, +1, +5, +7
Установите соответствие между формулой соли и продуктом, образующимися на катоде при электролизу водного раствора этой соли.
ФОРМУЛА СОЛИ
А) AgNO3
Б) Na2S
В) Ca(NO3)2
Г) CuCl2
ПРОДУКТ НА КАТОДЕ
1) водород
2) кислород
3) серебро
4) калий
5) кальций
6) медь
Установите соответствие между формулой соли и отношением этой соли к гидролизу.
ФОРМУЛА СОЛИ
А) CH3COOK
Б) Na2SO3
В) NH4Cl
Г) NaCl
ОТНОШЕНИЕ К ГИДРОЛИЗУ
1) гидролиз по катиону
2) гидролиз по аниону
3) гидролиз по катиону и аниону
4) гидролизу не подвергается
Установите соответствие между уравнением обратимой химической реакции и направлением смещения химического равновесия при увеличении давления в системе.
УРАВНЕНИЕ РЕАКЦИИ
А) 
Б) 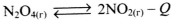
В) 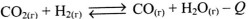
Г) 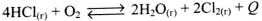
НАПРАВЛЕНИЕ СМЕШЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) смещается в сторону продуктов реакции
2) смещается в сторону исходных веществ
3) смещение равновесия не происходит
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать.
ФОРМУЛА ВЕЩЕСТВА
А) Zn(OH)2
Б) H2SO4 (разб.)
В) H2S
Г) Ca
РЕАГЕНТЫ
1) LiOH, HNO3, HCl
2) NaOH, K2O, CuSO4
3) H2O, S, HNO3
4) Zn, BaCl2, NaHS
5) NaNO3, CuO, SiO2
Установите соответствие между названиями двух веществ и реактивом, с помощью которого можно различить эти вещества.
НАЗВАНИЯ ВЕЩЕСТВ
А) этанол-1 и фенол (р-р)
Б) крахмал и сахароза (кр.)
В) пропанол-2 и глицерин
Г) толуол и бензол
РЕАКТИВ
1) NaMnO4 (р-р)
2) ZnO
3) Br2 (водн.)
4) Cu(OH)2
5) I2 (р-р)
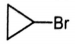
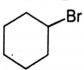
Установите соответствие углеводородом и продуктом, который преимущественно образуется при его взаимодействии с бромом.
НАЗВАНИЕ ВЕЩЕСТВА
А) этан
Б) изобутан
В) циклопропан
Г) циклогексан
ПРОДУКТ БРОМИРОВАНИЯ
1) 
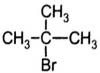
2) 
3) 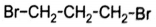
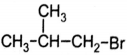
4) 
5) 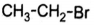
6) 
Установите соответствие между схемой реакции и веществом Х, которое является одним из реагентов в ней.
СХЕМА РЕАКЦИИ
А) фенол + Х → фенолят калия
Б) муравьиная кислота + Х → этилформиат
В) метаналь + Х → углекислый газ
Г) этанол + Х → этилат калия
ВЕЩЕСТВО Х
1) CH3OH
2) CuO
3) KMnO4(H+)
4) CH3CH2OH
5) KHCO3
6) K
Часть 2.
Запишите сначала номер задания (36, 37 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции:
KIO3 + KI + ... → I2 + K2SO4 + ...
Определите окислитель и восстановитель.
Элементы ответа:
1) Составлен электронный баланс:
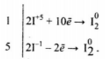
2) Указано, что иодид калия (за счет иода в степени окисления -1) является восстановителем, а иодат калия (за счет иода в степени окисления +5) - окислителем.
3) определены недостающие вещества, и расставлены коэффициенты в уравнении реакции:
KIO3 + 5KI + 3H2SO4 = 3I2 + 3K2SO4 + 3H2O
Цинк полностью растворили в концентрированном растворе гидроксида калия. Образовавшийся прозрачный раствор выпарили, а затем прокалили. Твердый остаток растворили в необходимом количестве соляной кислоты. К образовавшемуся прозрачному раствору добавили сульфид аммония и наблюдали образование белого осадка. Напишите уравнение четырех описанных реакций.
Ответ включает в себя 4 уравнение возможных реакций, соответствующих описанным превращениям:
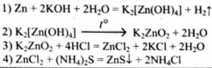
Напишите уравнение реакций, с помощью которых можно осуществить следующие превращения:
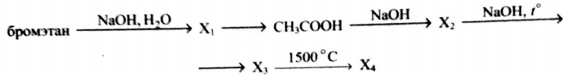
При написании уравнений реакций используйте структурные формулы органических веществ.
Ответ включает в себя 5 уравнений реакций, соответствующих схеме превращений:
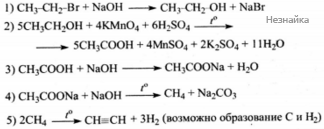
При сливании 160 г 10%-ного раствора нитрата бария и 50 г 11%-ного раствора хромата калия выпал осадок. Рассчитайте массовую долю нитрата бария в образовавшемся растворе.
Элементы ответа:
1) Записано уравнение реакции:
Ba(NO3)2 + K2CrO4 = BaCrO4↓ + 2KNO3
2) Рассчитаны количество вещества реагентов, и определено вещество, взятое в избытке:
n(Ba(NO3)2) = 160 x 0,1 / 261 = 0,061 моль
n(K2CrO4) = 50 x 0,11 / 194 = 0,028 моль
Ba(NO3)2 - в избытке
3) Рассчитаны масса выпавшего осадка и масса образовавшегося при этом раствора:
n(BaCrO4) = n(K2CrO4) = 0,028 моль
m(BaCrO4) = 0,028 моль х 253 г/моль = 7,08 г
m(раствора) = 160 + 50 - 7,08 = 202,92 г
4) Рассчитаны масса нитрата бария и его массовая доля в растворе:
n(Ba(NO3)2)изб = 0,061 - 0,028 = 0,033 моль
m(Ba(NO3)2) = 0,033 x 261 = 8,61 г
w(Ba(NO3)2) = m(Ba(NO3)2) / m(p-pa) = 8,61 / 202,92 = 0,042 или 4,2%
Некоторое органическое соединение содержит 40,0% углерода и 53,3% кислорода по массе. Известно, что это соединение реагирует с оксидом меди(II).
На основании данных условий задачи:
1. произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2. запишите молекулярную формулу органического вещества;
3. составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4. напишите уравнение реакции этого вещества с оксидом меди(II).
Элементы ответа:
Общая формула вещества - CxHyOz
1) Найдено соотношение атомов углерода, водорода и кислорода в соединении:
w(H) = 100 - 40,0 -53,3 = 6,7%
x : y : z = 40 / 12 : 6,7 / 1 : 53,3 / 16 = 3,33 : 6,7 : 3,33 = 1 : 2 : 1
2) Определена молекулярная формула вещества.
Простейшая формула вещества - CH2O. Учитывая то, что вещество реагирует с оксидом меди (II), молекулярная формула вещества - C2H4O2
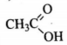
4) Составлено уравнение реакции с оксидом меди (II):
2CH3COOH + CuO → (CH3COO)2Cu + H2O
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||