Вариант 20
Часть 1.
Ответом к заданиям 1–26 является последовательность цифр. Цифры в ответах на задания 5, 10–12, 18, 19, 22–26 могут повторяться.
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют на внешнем энергетическом уровне два электрона. Запишите в поле ответа номера выбранных элементов.
1. Mg
2. S
3. Ti
4. Al
5. Ne
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде. Расположите выбранные элементы в порядке уменьшения их металлических свойств. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
1. Mg
2. S
3. Ti
4. Al
5. Ne
Из числа указанных в ряду элементов выберите два элемента, которые проявляют степень окисления, равную +4. Запишите в поле ответа номера выбранных элементов.
1. Mg
2. S
3. Ti
4. Al
5. Ne
Из предложенного перечня выберите два соединения, в которых присутствует ковалентная полярная химическая связь.
1. CaO
2. HCIO
3. N2
4. HCl
5. LiCl
Установите соответствие между формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) Cr2O3
Б) CrO3
В) CrO
КЛАСС/ГРУППА
1) кислотный оксид
2) основный оксид
3) амфотерный оксид
4) несолеобразующий оксид
Из предложенного перечня веществ выберите два вещества, с каждым из которых реагирует фосфор.
1) концентрированная азотная кислота
2) концентрированная соляная кислота
3) бром
4) водород
5) хлорид железа(II) (р-р)
Из предложенного перечня выберите два оксида, которые при обычных условиях реагируют с раствором гидроксида натрия, но не реагируют с азотной кислотой.
1. N2O5
2. CO2
3. FeO
4. NO
5. ZnO
В пробирку с раствором вещества X добавили несколько капель раствора кислоты Y. В результате реакции наблюдали выделение бесцветного газа. Из предложенного перечня выберите два вещества, которые могут вступать в описанную реакцию.
1. H2SiO3
2. H2SO4
3. NH4Cl
4. CaCO3
5. (NH4)2S
Задана следующая схема превращений веществ:
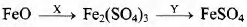
Определите, какие из указанных веществ являются веществами Хи Y.
1. Fe
2. H2SO4 (разб.)
3. NH3 (p-p)
4. H2SO4 (конц.)
5. Br2 (p-p)
Установите соответствие между уравнением реакции и свойством элемента серы, которое она проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УРАВНЕНИЕ РЕАКЦИИ
А) Са + S = CaS
Б) SO2 + КОН = KHSO3
В) S + O2 = SO2
Г) 3S + 6КОН = 2K2S + K2SO3 + 3H2O
СВОЙСТВО СЕРЫ
1) является окислителем
2) является восстановителем
3) является и окислителем, и восстановителем
4) не проявляет окислительно-восстановительных свойств
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) O2
Б) P2O5
В) Al(OH)3
Г) MgBr2
РЕАГЕНТЫ
1) NaOH, СаО, Н2O
2) КОН, AgNO3, NH3 H2O
3) NH3 H20, SiO2, CH3COOH
4) КОН, SO3, HNO3
5) SO2,CO,K2SO3
Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) глицерин
Б) глицин
В) стирол
КЛАСС/ГРУППА
1) альдегиды
2) спирты
3) аминокислоты
4) углеводороды
Из предложенного перечня веществ выберите два вещества, которые являются изомерами этилацетата:
1) уксусная кислота
2) бутановая кислота
3) пропановая кислота
4) изопропиловый эфир муравьиной кислоты
5) пропиловый эфир уксусной кислоты
Из предложенного перечня выберите два вещества, каждое из которых реагирует с раствором перманганата калия.
1) циклогексан
2) дивинил
3) 2-метилгексан
4) пропан
5) циклогексен
Из предложенного перечня выберите два вещества, с которыми взаимодействует этаналь.
1) водород
2) гидроксид меди(II)
3) гидроксид железа(II)
4) бутан
5) оксид алюминия
Из предложенного перечня выберите два вещества, с которыми взаимодействует глицин.
1) гидроксид натрия
2) угарный газ
3) соляная кислота
4) медь
5) метан
Задана следующая схема превращений веществ:
этаналь → Y → уксусная кислота → X → метан
Определите, какие из указанных веществ являются веществами Хи Y.
1. этанол
2. CH3COONa
3. 1,2-дихлорэтан
4. Cu(OH)2
5. H2SO4 ([math]t^\circ[/math])
Установите соответствие между названием реакции и её преимущественным продуктом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ РЕАКЦИИ
А) пиролиз метана
Б) гидрирование бензола
В) гидрирование циклопропана
Г) дегидрирование пропана
ПРОДУКТ РЕАКЦИИ
1) метанол
2) пропен
3) пропан
4) циклопропан
5) ацетилен
6) циклогексан
Установите соответствие между схемой реакции и реагентом X, который принимает в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) фенол → X → циклогексанол
Б) этаналь → X → уксусная кислота
В) толуол → X → бензоат калия
Г) этанол → X → уксусная кислота
РЕАГЕНТ X
1) CuO
2) H2 (кат.)
3) KOH
4) KMnO4 (водн.)
5) KMnO4 (H+)
6) H2SO4 (конц.)
Из предложенного перечня типов реакций выберите два типа, к которым можно отнести взаимодействие метана с хлором.
1) каталитическая
2) гомогенная
3) обратимая
4) окислительно-восстановительная
5) реакция нейтрализации
Из предложенного перечня внешних воздействий выберите два, которые приводят к уменьшению скорости реакции цинка с серной кислотой.
1) понижение температуры
2) измельчение цинка
3) использование катализатора
4) уменьшение концентрации кислоты
5) понижение давления в системе
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) Al2(SO4)3
Б) ВаВг2
В) Cu(NO3)2
Г) AgF
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и сера
2) водород и кислород
3) металл и галоген
4) металл и кислород
5) водород и галоген
Установите соответствие между названием соли и отношением этой соли к гидролизу: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ СОЛИ
А) бромид аммония
Б) стеарат натрия
В) перхлорат натрия
Г) сульфид аммония
ОТНОШЕНИЕ К ГИДРОЛИЗУ
1) гидролизуется по катиону
2) гидролизуется по аниону
3) гидролизу не подвергается
4) гидролизуется по катиону и аниону
Установите соответствие между способом воздействия на равновесную систему
2СО(г) + О2(г) [math]\leftrightarrows[/math] 2СО2(г) + Q
и направлением смещения химического равновесия в результате этого воздействия: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца.
ВОЗДЕЙСТВИЕ НА СИСТЕМУ
А) уменьшение концентрации оксида углерода(II)
Б) уменьшение концентрации кислорода
В) увеличение давления
Г) увеличение температуры
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) в сторону продуктов реакции
2) в сторону исходных веществ
3) практически не смещается
Установите соответствие между формулами веществ и реагентом, с помощью которого можно их различить: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛЫ ВЕЩЕСТВ
А) пропан и пропен
Б) пропанол-1 и глицерин
В) пропанол-2 и пропионовая кислота
Г) фруктоза (р-р) и этанол
РЕАГЕНТ
1) Сu(ОН)2
2) Br2 (p-p)
3) C2H5OH
4) NaCl
5) H2SO4
Установите соответствие между веществом и областью его применения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) фосфорная кислота
Б) метан
В) ацетон
Г) кокс
ОБЛАСТЬ ПРИМЕНЕНИЯ
1) получение удобрений
2) в качестве топлива
3) в качестве растворителя
4) производство чугуна
5) получение полимеров
К 105 г раствора с массовой долей хлорида натрия 10% добавили 40 мл воды и 10 г соли. Определите массовую долю соли в полученном растворе.
Ответ:____________________%.
(Запишите число с точностью до десятых.)
Определите количество теплоты, которая выделится при образовании 90 г воды в соответствии с термохимическим уравнением
СH4 + 2O2 = СO2 + 2Н2O + 892 кДж
Ответ:___________________кДж.
(Запишите число с точностью до целых.)
Вычислите массу кислорода (в граммах), необходимого для окисления 6,72 л (н.у.) аммиака до азота.
Ответ:___________________г.
(Запишите число с точностью до десятых.)
Часть 2.
Запишите сначала номер задания (30, 31 и т. д.), затем подробное решение. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции
Cr(NO3)3 + ... + NaOH → Na2CrO4 + ... + NaBr + H2O
Определите окислитель и восстановитель.
Электронный баланс:
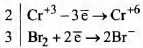
Окислитель Вг2, восстановитель Сг+3 (или Сг(NO3)3)
Уравнение реакции: 2Сг(NO3)3 + ЗВг2 + 16NaOH → 2Na2CrO4 + 6NaNO3 + 6NaBr + 8Н2O
Гидроксид хрома(III) обработали в щелочной среде хлором. Полученный жёлтый раствор после подкисления серной кислотой измененил цвет на оранжевый. Соль, образовавшуюся в растворе, выделили и нагрели с концентрированной бромоводородной кислотой. Образовавшееся при этом простое вещество растворили в тёплом растворе едкого натра. Напишите уравнения четырёх описанных реакций.
1) 2Сг(ОН)3 + 10КОН + ЗСl2 = 2К2СrO4 + 6КСl + 8Н2O
2) 2К2СrO4 + H2SO4 = К2Сг2O7 + K2SO4 + Н2O
3) К2Сг2O7 + 14НВг = 2СrВг3 + 2КВг + ЗВг2 + 7Н2O
4) 3Br2 + 6NaOH = 5NaBr + NaBrO3 + 3H2O
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
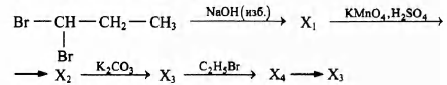
При написании уравнений реакций используйте структурные формулы органических веществ.
1) СН3—СН2—CHBr2 + 2NaOH → 2NaBr + Н2O + СН3—СН2—С(O)Н
2) 5СН3—СН2—С(O)Н + 2КМnO4 + 3H2SO4 → 5СН3—СН2—СООН + 2MnSO4 + K2SO4 + 3H2O
3) 2СН3—СН2—СООН + К2СO3 → 2СН3—СНr—COOK + СO2 + Н2O
4) СН3—СНr—COOK + С2Н5Вг → СН3—СНг—СОО—С2Н5 + КВг
5) СН3—СН2—СОО—С2Н5 + КОН → СН3—СНг—COOK + С2Н5ОН
Твёрдый остаток, полученный при взаимодействии 4,48 л (н.у.) водорода с 24 г оксида меди(II), растворили в 250 г 75%-ного раствора азотной кислоты. Определите массовую долю азотной кислоты в образовавшемся растворе.
w(HNO3) = 0,494 или 49,4%.
При сгорании 12,6 г органического вещества, в молекуле которого содержится один третичный атом углерода, получили 20,16 л (н.у.) углекислого газа и 16,2 г воды. Относительная плотность паров этого вещества по углекислому газу равна 1,909. Известно, что это вещество не взаимодействует с водой, но реагирует с бромом на свету.
На основании данных условия задания:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу исходного органического вещества;
3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение взаимодействия данного вещества с бромом.
2) молекулярная формула вещества C6H12
3) структурная формула 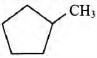
4) уравнение реакции 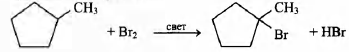
| № | Ваш ответ | Ответ и решение | Первичный балл |
|---|---|---|---|
|
Здесь появится результат первой части. Нажмите на кнопку «Завершить работу», чтобы увидеть правильные ответы и посмотреть решения. |
|||